スペイン風邪
Spanish flu
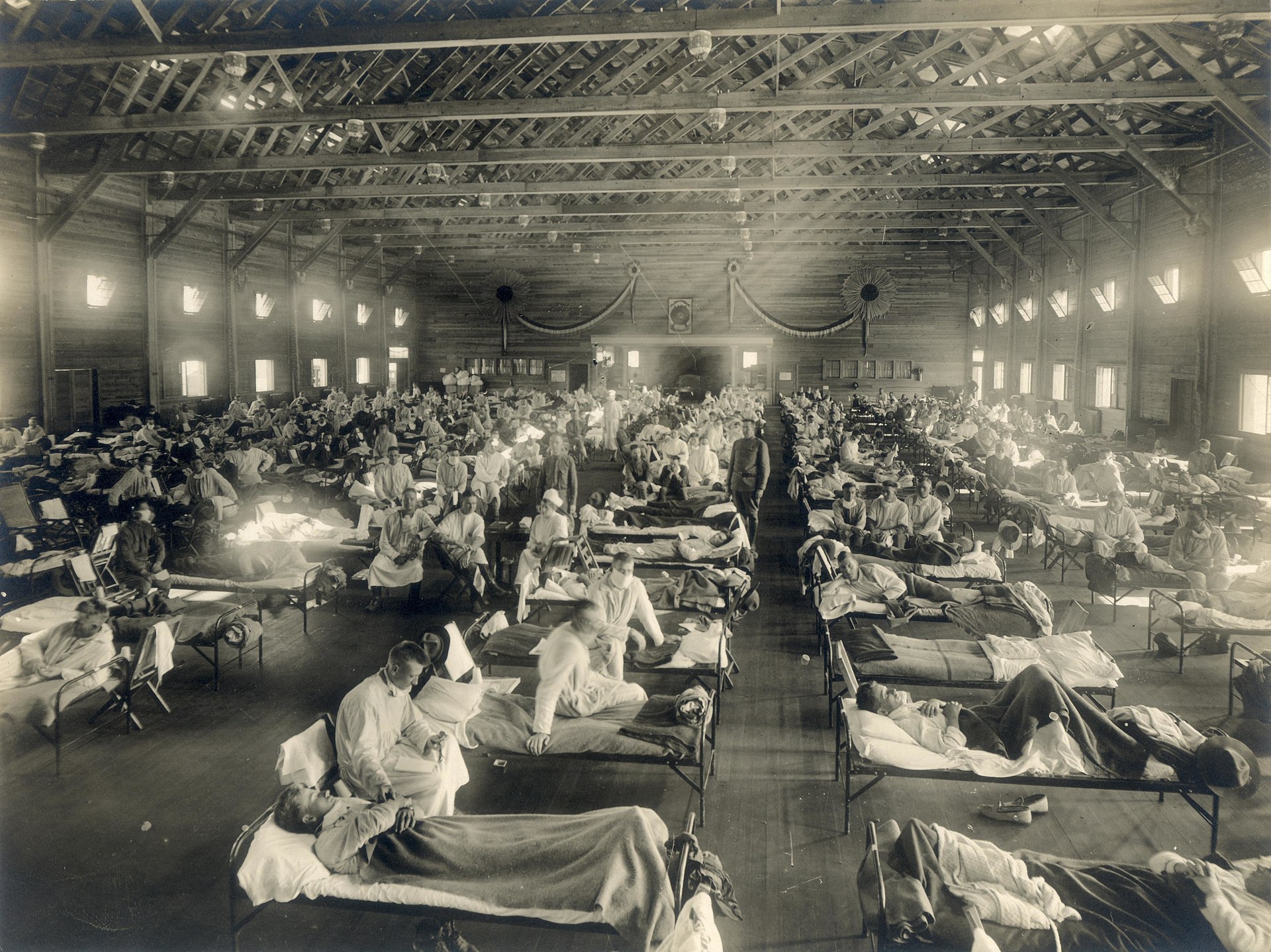
Soldiers sick with Spanish flu at a hospital ward at Camp Funston in Fort Riley, Kansas
☆1918
年から1920年にかけて発生したインフルエンザの大流行は、スペイン風邪とも呼ばれるが、これはインフルエンザAウイルスのH1N1亜型によって引き起
こされた、きわめて致死率の高い世界的なインフルエンザのパンデミックであった。
記録に残る最初の症例は1918年3月に米国カンザス州で発生し、4月にはフランス、ドイツ、英国でも症例が記録された。2年後には、4つの波にわたって
世界人口のほぼ3分の1にあたる5億人が感染した。
死亡者数は1700万人から5000万人と推定されており[6][7]、1億人に達する可能性もある[8]。
このパンデミックは、第一次世界大戦の終戦間近に勃発した。交戦国では戦時中の検閲官が士気を維持するために悪いニュースを抑制したが、中立国スペインで
は新聞が自由に発生を報道したため、スペインが流行の中心地であるという誤った印象が生まれ、「スペイン風邪」という誤称につながった。[9]
限られた歴史的疫学データにより、パンデミックの地理的発生源は特定できず、初期の感染拡大に関する仮説は競合している。[2]
ほとんどのインフルエンザの流行では、若年層と高齢層が不均衡に死亡し、その中間の年齢層では生存率が高いが、このパンデミックでは若い成人層の死亡率が
異常に高かった。[10]
科学者たちは、この高い死亡率について、6年間にわたる気候の異常が、水系感染による拡大の可能性を高め、病気の媒介動物の移動に影響を与えたことなど、
いくつかの説明を提示している。[11] しかし、このパンデミックで若い成人の死亡率が高かったという主張は異論もある。[12]
栄養失調、過密状態の医療キャンプや病院、そして戦争によって悪化した不衛生な環境が細菌の二次感染を促進し、犠牲者のほとんどが典型的な長引く死床の後
に死亡した。[13][14]
1918年のスペイン風邪は、H1N1型インフルエンザウイルスによって引き起こされた3つのインフルエンザ・パンデミックの最初のものだった。他の2つ
は、1977年のロシア風邪と2009年の豚インフルエンザ・パンデミックである。
| The 1918–1920 flu
pandemic, also known as the Great Influenza epidemic or by the common
misnomer Spanish flu, was an exceptionally deadly global influenza
pandemic caused by the H1N1 subtype of the influenza A virus. The
earliest documented case was March 1918 in the state of Kansas in the
United States, with further cases recorded in France, Germany and the
United Kingdom in April. Two years later, nearly a third of the global
population, or an estimated 500 million people, had been infected in
four successive waves. Estimates of deaths range from 17 million to 50
million,[6][7] and possibly as high as 100 million,[8] making it one of
the deadliest pandemics in history. The pandemic broke out near the end of World War I, when wartime censors in the belligerent countries suppressed bad news to maintain morale, but newspapers freely reported the outbreak in neutral Spain, creating a false impression of Spain as the epicenter and leading to the "Spanish flu" misnomer.[9] Limited historical epidemiological data make the pandemic's geographic origin indeterminate, with competing hypotheses on the initial spread.[2] Most influenza outbreaks disproportionately kill the young and old, with a higher survival rate in-between, but this pandemic had unusually high mortality for young adults.[10] Scientists offer several explanations for the high mortality, including a six-year climate anomaly affecting migration of disease vectors with increased likelihood of spread through bodies of water.[11] However, the claim that young adults had a high mortality during the pandemic has been contested.[12] Malnourishment, overcrowded medical camps and hospitals, and poor hygiene, exacerbated by the war, promoted bacterial superinfection, killing most of the victims after a typically prolonged death bed.[13][14] The 1918 Spanish flu was the first of three flu pandemics caused by H1N1 influenza A virus; the others being the 1977 Russian flu and the 2009 Swine flu pandemics.[15][16][17] |
1918年から1920年にかけて発生したインフルエンザの大流行は、
スペイン風邪とも呼ばれるが、これはインフルエンザAウイルスのH1N1亜型によって引き起こされた、きわめて致死率の高い世界的なインフルエンザのパン
デミックであった。
記録に残る最初の症例は1918年3月に米国カンザス州で発生し、4月にはフランス、ドイツ、英国でも症例が記録された。2年後には、4つの波にわたって
世界人口のほぼ3分の1にあたる5億人が感染した。
死亡者数は1700万人から5000万人と推定されており[6][7]、1億人に達する可能性もある[8]。 このパンデミックは、第一次世界大戦の終戦間近に勃発した。交戦国では戦時中の検閲官が士気を維持するために悪いニュースを抑制したが、中立国スペインで は新聞が自由に発生を報道したため、スペインが流行の中心地であるという誤った印象が生まれ、「スペイン風邪」という誤称につながった。[9] 限られた歴史的疫学データにより、パンデミックの地理的発生源は特定できず、初期の感染拡大に関する仮説は競合している。[2] ほとんどのインフルエンザの流行では、若年層と高齢層が不均衡に死亡し、その中間の年齢層では生存率が高いが、このパンデミックでは若い成人層の死亡率が 異常に高かった。[10] 科学者たちは、この高い死亡率について、6年間にわたる気候の異常が、水系感染による拡大の可能性を高め、病気の媒介動物の移動に影響を与えたことなど、 いくつかの説明を提示している。[11] しかし、このパンデミックで若い成人の死亡率が高かったという主張は異論もある。[12] 栄養失調、過密状態の医療キャンプや病院、そして戦争によって悪化した不衛生な環境が細菌の二次感染を促進し、犠牲者のほとんどが典型的な長引く死床の後 に死亡した。[13][14] 1918年のスペイン風邪は、H1N1型インフルエンザウイルスによって引き起こされた3つのインフルエンザ・パンデミックの最初のものだった。他の2つ は、1977年のロシア風邪と2009年の豚インフルエンザ・パンデミックである。 |
Etymologies El Sol (Madrid), 28 May 1918: "The three-day fever – In Madrid 80,000 Are Infected – H.M. the King is sick" This pandemic was known by many different names—some old, some new—depending on place, time, and context. The etymology of alternative names historicises the scourge and its effects on people who would only learn years later that invisible viruses caused influenza.[18] The lack of scientific answers led the Sierra Leone Weekly News (Freetown) to suggest a biblical framing in July 1918, using an interrogative from Exodus 16 in ancient Hebrew:[a] "One thing is for certain—the doctors are at present flabbergasted; and we suggest that rather than calling the disease influenza they should for the present until they have it in hand, say Man hu—'What is it?'"[20][21][22] Descriptive names Outbreaks of influenza-like illness were documented in 1916–17 at British military hospitals in Étaples, France,[23] and just across the English Channel at Aldershot, England. Clinical indications in common with the 1918 pandemic included rapid symptom progression to a "dusky" heliotrope cyanosis of the face. This characteristic blue-violet cyanosis in expiring patients led to the name 'purple death'.[24][25][26] The Aldershot physicians later wrote in The Lancet, "the influenza pneumococcal purulent bronchitis we and others described in 1916 and 1917 is fundamentally the same condition as the influenza of this present pandemic."[27] This "purulent bronchitis" is not yet linked to the same A/H1N1 virus,[28] but it may be a precursor.[27][29][30] In 1918, 'epidemic influenza' (Italian: influenza, influence),[31] also known at the time as 'the grip' (French: la grippe, grasp),[32] appeared in Kansas in the U.S. during late spring, and early reports from Spain began appearing on 21 May.[33][34] Reports from both places called it 'three-day fever' (fiebre de los tres días).[35][36][37] Associative names  Front page of The Times (London), 25 June 1918: "The Spanish Influenza" Many alternative names are exonyms in the practice of making new infectious diseases seem foreign.[38][39][40] This pattern was observed even before the 1889–1890 pandemic, also known as the 'Russian flu', when the Russians already called epidemic influenza the 'Chinese catarrh', the Germans called it the 'Russian pest', while the Italians in turn called it the 'German disease'.[41][42] These epithets were re-used in the 1918 pandemic, along with new ones.[43] 'Spanish' influenza  Advertisement in The Times, 28 June 1918 for Formamint tablets to prevent "Spanish influenza" Outside Spain, the disease was soon misnamed 'Spanish influenza'.[44][45] In a 2 June 1918 The Times of London dispatch titled, "The Spanish Epidemic," a correspondent in Madrid reported over 100,000 victims of, "The unknown disease…clearly of a gripal character," without referring to "Spanish influenza" directly.[46] Three weeks later The Times reported that, "Everybody thinks of it as the 'Spanish' influenza to-day."[47] Three days after that an advertisement appeared in The Times for Formamint tablets to prevent "Spanish influenza".[48][49] When it reached Moscow, Pravda announced, "Ispánka (the Spanish lady) is in town," making 'the Spanish lady' another common name.[50] The outbreak did not originate in Spain (see below),[51] but reporting did, due to wartime censorship in belligerent nations. Spain was a neutral country unconcerned with appearances of combat readiness, and without a wartime propaganda machine to prop up morale;[52][53] so its newspapers freely reported epidemic effects, including King Alfonso XIII's illness, making Spain the apparent locus of the epidemic.[54] The censorship was so effective that Spain's health officials were unaware its neighboring countries were similarly affected.[55] In an October 1918 "Madrid Letter" to the Journal of the American Medical Association, a Spanish official protested, "we were surprised to learn that the disease was making ravages in other countries, and that people there were calling it the 'Spanish grip'. And wherefore Spanish? …this epidemic was not born in Spain, and this should be recorded as a historic vindication."[56] But before this letter could be published, The Serbian Newspaper (Corfu) said, "Various countries have been assigning the origin of this imposing guest to each other for quite some time, and at one point in time they agreed to assign its origin to the kind and neutral Spain…"[57]  "Spanish influenza," "three-day fever," "the flu." by Rupert Blue, U.S. Surgeon General, 28 September 1918 Other exonyms French press initially used 'American flu', but adopted 'Spanish flu' in lieu of antagonizing an ally.[58] In the spring of 1918, British soldiers called it 'Flanders flu', while German soldiers used 'Flandern-Fieber' (Flemish fever), both after a famous battlefield in Belgium where many soldiers on both sides fell ill.[43][40][59][60] In Senegal it was named 'Brazilian flu', and in Brazil, 'German flu'.[61] In Spain it was also known as the 'French flu' (gripe francesa),[51][9] or the 'Naples Soldier' (Soldado de Nápoles), after a popular song from a zarzuela.[b][58] Spanish flu (gripe española) is now a common name in Spain,[63] but remains controversial there.[64][65] Other names derived from geopolitical borders and social boundaries. In Poland it was the 'Bolshevik disease',[61][66] while the Bolsheviks referred to it as the 'Kirghiz disease'.[60] Some Africans called it a 'white man's sickness', but in South Africa, white men also used the ethnophaulism 'kaffersiekte' (lit. negro disease).[43][67] Japan blamed sumo wrestlers for bringing the disease home from a match in Taiwan by calling it 'sumo flu' (Sumo Kaze), even though three top wrestlers died there.[68][69] World Health Organization 'best practices' first published in 2015 now aim to prevent social stigma by no longer associating culturally significant names with new diseases, listing "Spanish flu" under "examples to be avoided".[70][39][71] Many authors now eschew calling this the Spanish flu,[58] instead using variations of '1918–19/20 flu/influenza pandemic'.[72][73][74] Local names Some language endonyms did not name specific regions or groups of people. Examples specific to this pandemic include: Northern Ndebele: 'Malibuzwe' (let enquiries be made concerning it), Swahili: 'Ugonjo huo kichwa na kukohoa na kiuno' (the disease of head and coughing and spine),[75] Yao: 'chipindupindu' (disease from seeking to make a profit in wartime), Otjiherero: 'kaapitohanga' (disease which passes through like a bullet),[76] and Persian: 'nakhushi-yi bad' (disease of the wind).[77][78] Other names This outbreak was also commonly known as the 'great influenza epidemic',[79][80] after the 'great war', a common name for World War I before World War II.[81] French military doctors originally called it 'disease 11' (maladie onze).[40] German doctors downplayed the severity by calling it 'pseudo influenza' (Latin: pseudo, false), while in Africa, doctors tried to get patients to take it more seriously by calling it 'influenza vera' (Latin: vera, true).[82] A children's song from the 1889–90 flu pandemic[83] was shortened and adapted into a skipping-rope rhyme popular in 1918.[84][85] It is a metaphor for the transmissibility of 'Influenza', where that name was clipped to the apheresis 'Enza':[86][87][88] I had a little bird, its name was Enza. I opened the window, and in-flu-enza. |
語源 1918年5月28日付『エル・ソル』(マドリード)紙:「3日熱 - マドリードで8万人が感染 - 王陛下もご病気」 このパンデミックは、場所や時代、文脈によって、古いものから新しいものまで、さまざまな名称で呼ばれた。 代替名称の語源は、この惨事と、目に見えないウイルスがインフルエンザを引き起こしていることを何年も後に知ることになる人々への影響を歴史的に物語って いる。[18] 科学的な回答が得られないことから、シエラレオネ・ウィークリーニュース(フリータウン)は1918年7月、古代ヘブライ語の『出エジプト記』第16章か らの疑問文を用いて、聖書的な枠組みを提案した 「確かなことはただ一つ、医師たちは今、当惑しているということだ。そして、この病気をインフルエンザと呼ぶよりも、彼らがこの病気を手に負えるようにな るまでは、マンフ(Man hu)『これは何だ?』と呼ぶべきだと我々は提案する」[20][21][22] 記述的な名称 1916年から1917年にかけて、フランス、エタプルのイギリス軍病院[23]、および英仏海峡を隔てたイングランドのアルダショットで、インフルエン ザ様疾患の発生が記録されている。1918年のパンデミックと共通する臨床症状には、急速な症状進行により、顔面が「青みがかった」ヘリオトロープチア ノーゼになることが含まれていた。この特徴的な青紫色のチアノーゼは、死亡する患者にみられ、「紫の死」という名称につながった。[24][25] [26] アルダーショットの医師らは後に『ランセット』誌に「1916年と1917年に我々や他の者たちが記述したインフルエンザ連鎖球菌性化膿性気管支炎は、基 本的に今回のパンデミックのインフルエンザと同じ状態である」と記している。[27] この「化膿性気管支炎」は、まだ同じA/H1N1ウイルスと関連付けられてはいないが、[28] 前兆である可能性はある。[27][29][30] 1918年、当時「流行性感冒」(イタリア語:インフルエンザ、影響)[31]、「流行性感冒」(フランス語:ラ・グリップ、把握)[32]として知られ ていた「流行性感冒」が、 。春の終わり頃にアメリカ合衆国のカンザス州で発生し、5月21日にはスペインからの初期の報告が現れ始めた。[33][34] 両地域からの報告では「3日熱(fiebre de los tres días)」と呼ばれていた。[35][36][37] 関連名称  1918年6月25日付のロンドン・タイムズ紙の第一面:「スペイン風邪」 多くの代替名称は、新しい感染症を外国由来のもののように見せるための外来語である。[38][39][40] このパターンは、1889年から1890年にかけてのパンデミック(「ロシア風邪」とも呼ばれる)以前にも見られた。当時、ロシアではすでに流行性インフ ルエンザを 「中国カタル」と呼び、ドイツ人は「ロシアの疫病」と呼び、イタリア人は「ドイツの病気」と呼んだ。[41][42] これらの異名は、1918年のパンデミックでも、新しい異名とともに再び使用された。[43] 「スペイン風」インフルエンザ  1918年6月28日付のタイムズ紙の広告。「スペイン風」インフルエンザを予防するFormamint錠剤 スペイン国外では、この病気はすぐに「スペイン風邪」と誤って呼ばれるようになった。[44][45] 1918年6月2日付のロンドン・タイムズ紙の「スペインの疫病」と題された記事では、マドリード特派員が「原因不明の病気…明らかに風邪のような症状」 により10万人以上の犠牲者が出ていると報告したが、「スペイン風邪」という言葉は直接には用いられていない。[46] 3週間後、 タイムズ紙は「今日では誰もがそれを『スペイン風』インフルエンザと呼んでいる」と報じた。[47] その3日後には、タイムズ紙に「スペイン風」インフルエンザを予防するFormamint錠の広告が掲載された。[48][49] モスクワに到達した際には、プラウダが「イスパンカ(スペインの女性)が街にいる」と報じ、「スペインの女性」という呼び名も一般的になった。[50] この流行はスペインで発生したものではなかったが(下記参照)[51]、交戦国における戦時中の検閲により、報道は行われた。スペインは中立国であり、戦 闘準備態勢の体裁には関心がなく、戦時下における国民の士気を高揚させるためのプロパガンダの仕組みもなかったため[52][53]、スペインの新聞は流 行病の影響を自由に報道し、アルフォンソ13世の病気も報道したため、スペインが流行病の中心地であるかのように見えた[54]。検閲は非常に効果的であ り、スペインの保健当局は近隣諸国でも同様に流行病が流行していることを知らなかった[55]。 1918年10月、スペインの当局者は、米国医師会誌に寄せた「マドリード便り」の中で、「この病気が他の国々で猛威を振るい、人々がそれを『スペイン風 邪』と呼んでいることを知って驚いた。なぜスペイン風邪なのか?この流行はスペインで発生したものではない。これは歴史的な正当性として記録されるべきで ある」[56] しかし、この手紙が発表される前に、セルビア新聞(コルフ)は次のように伝えている。「この堂々たる来訪者の発生源については、さまざまな国が互いに主張 し合ってきたが、ある時点で、その発生源を親切で中立的なスペインに帰するということで合意した」[57]  「スペイン風邪」、「3日熱」、「インフルエンザ」 1918年9月28日、米国公衆衛生局長官ルパート・ブルー その他の呼称 当初、フランスは「アメリカ風邪」と呼んでいたが、同盟国を刺激しないよう「スペイン風邪」という呼称を採用した。[58] 1918年の春、イギリス兵はこれを「フランダース風邪」と呼び、ドイツ兵は「フランダース熱」(フランドル熱)と呼んだ。これは、両軍の多くの兵士が倒 れたベルギーの有名な戦場にちなんで名付けられたものである。[43][40][59][60] セネガルでは「ブラジル風邪」と呼ばれ 、ブラジルでは「ドイツ風邪」と呼ばれた。[61] スペインでは「フランス風邪」(gripe francesa)[51][9]、またはスペインのサルスエラの人気曲にちなんで「ナポリの兵士」(Soldado de Nápoles)とも呼ばれた。[b][58] スペイン風邪(gripe española)は現在ではスペインでの一般的な名称であるが[63]、スペインでは依然として論争の的となっている。[64][65] 他の名称は、地政学上の境界や社会的な境界から派生した。ポーランドでは「ボルシェビキ病」と呼ばれたが[61][66]、一方、ボルシェビキは「キルギ ス病」と呼んでいた[60]。一部のアフリカ人は「白人の病気」と呼んだが、南アフリカでは白人も民族主義的な用語である 「kaffersiekte」(文字通りには「黒人病」)と呼んでいた。[43][67] 日本では、台湾での試合から持ち帰った病気を「相撲風邪」(Sumo Kaze)と呼び、力士たちを非難した。 2015年に初めて発表された世界保健機関の「ベストプラクティス」は、現在では、文化的に重要な名称を新たな疾患と関連付けることをやめることで社会的 スティグマを防止することを目的としており、「スペイン風邪」を「避けるべき例」として挙げている。[70][3 9][71] 現在では、これをスペイン風邪と呼ぶことを避ける著者が多くなっており、代わりに「1918–19/20年のインフルエンザ/インフルエンザ・パンデミッ ク」のバリエーションが使用されている。[72][73][74] 地域名 言語のエンドネームの中には、特定の地域や人々を指さないものもある。今回のパンデミックに特有の例としては、北ンデベレ語:「Malibuzwe」(問 い合わせをさせてください)、スワヒリ語:「Ugonjo huo kichwa na kukohoa na kiuno」(頭と咳と背骨の病気)[75]、ヤオ語:「chipindupindu (戦時中に利益を得ようとして起こる病気)、オジ・ヘレロ語:『kaapitohanga』(弾丸のように伝播する病気)[76]、ペルシア語: 『nakhushi-yi bad』(風の病気)[77][78]などである。 その他の名称 この流行は、第一次世界大戦を指す「大戦」という通称にちなんで、「大インフルエンザ流行」とも呼ばれた。[79][80] フランス軍の軍医たちは当初、この病気を「11番目の病気」(maladie onze)と呼んでいた。 [40] ドイツの医師たちは「疑似インフルエンザ」(ラテン語:疑似、偽)と呼んでその深刻さを軽視したが、一方でアフリカでは医師たちが「真性インフルエンザ」 (ラテン語:真性、真)と呼んで患者にそれをより深刻に受け止めるよう促していた。[82] 1889年から1890年にかけてのインフルエンザ大流行の際に歌われた子供向けの歌[83]が短縮され、1918年に縄跳びの唄として人気を博した [84][85]。これは「インフルエンザ」の感染力を比喩的に表現したもので、この名称は「エンザ」というアフェレーシスに短縮された[86][87] [88]。 私は小鳥を飼っていた。 その名はエンザ。 窓を開けると、 インフルエンザ。 |
| History Timeline First wave of early 1918  Seattle policemen wearing cloth face masks handed out by the American Red Cross during the Spanish flu pandemic, December 1918 The pandemic is conventionally marked as having begun on 4 March 1918 with the recording of the case of Albert Gitchell, an army cook at Camp Funston in Kansas, United States, despite there having been cases before him.[89] The disease had already been observed 200 miles (320 km) away in Haskell County as early as January 1918, prompting local doctor Loring Miner to warn the editors of the U.S. Public Health Service's academic journal Public Health Reports.[81] Within days of the 4 March first case at Camp Funston, 522 men at the camp had reported sick.[90] By 11 March 1918, the virus had reached Queens, New York.[91] Failure to take preventive measures in March/April was later criticized.[92] As the U.S. had entered World War I, the disease quickly spread from Camp Funston, a major training ground for troops of the American Expeditionary Forces, to other U.S. Army camps and Europe, becoming an epidemic in the Midwest, East Coast, and French ports by April 1918, and reaching the Western Front by the middle of the month.[89] It then quickly spread to the rest of France, Great Britain, Italy, and Spain and in May reached Wrocław and Odessa.[89] After the signing of the Treaty of Brest-Litovsk (March 1918), Germany started releasing Russian prisoners of war, who then brought the disease to their country.[93] It reached North Africa, India, and Japan in May, and soon after had likely gone around the world as there had been recorded cases in Southeast Asia in April.[94] In June an outbreak was reported in China.[95] After reaching Australia in July, the wave started to recede.[94] The first wave of the flu lasted from the first quarter of 1918 and was relatively mild.[96] Mortality rates were not appreciably above normal;[2] in the United States ~75,000 flu-related deaths were reported in the first six months of 1918, compared to ~63,000 deaths during the same time period in 1915.[97] In Madrid, Spain, fewer than 1,000 people died from influenza between May and June 1918.[98] There were no reported quarantines during the first quarter of 1918. However, the first wave caused a significant disruption in the military operations of World War I, with three-quarters of French troops, half the British forces, and over 900,000 German soldiers sick.[99] Deadly second wave of late 1918 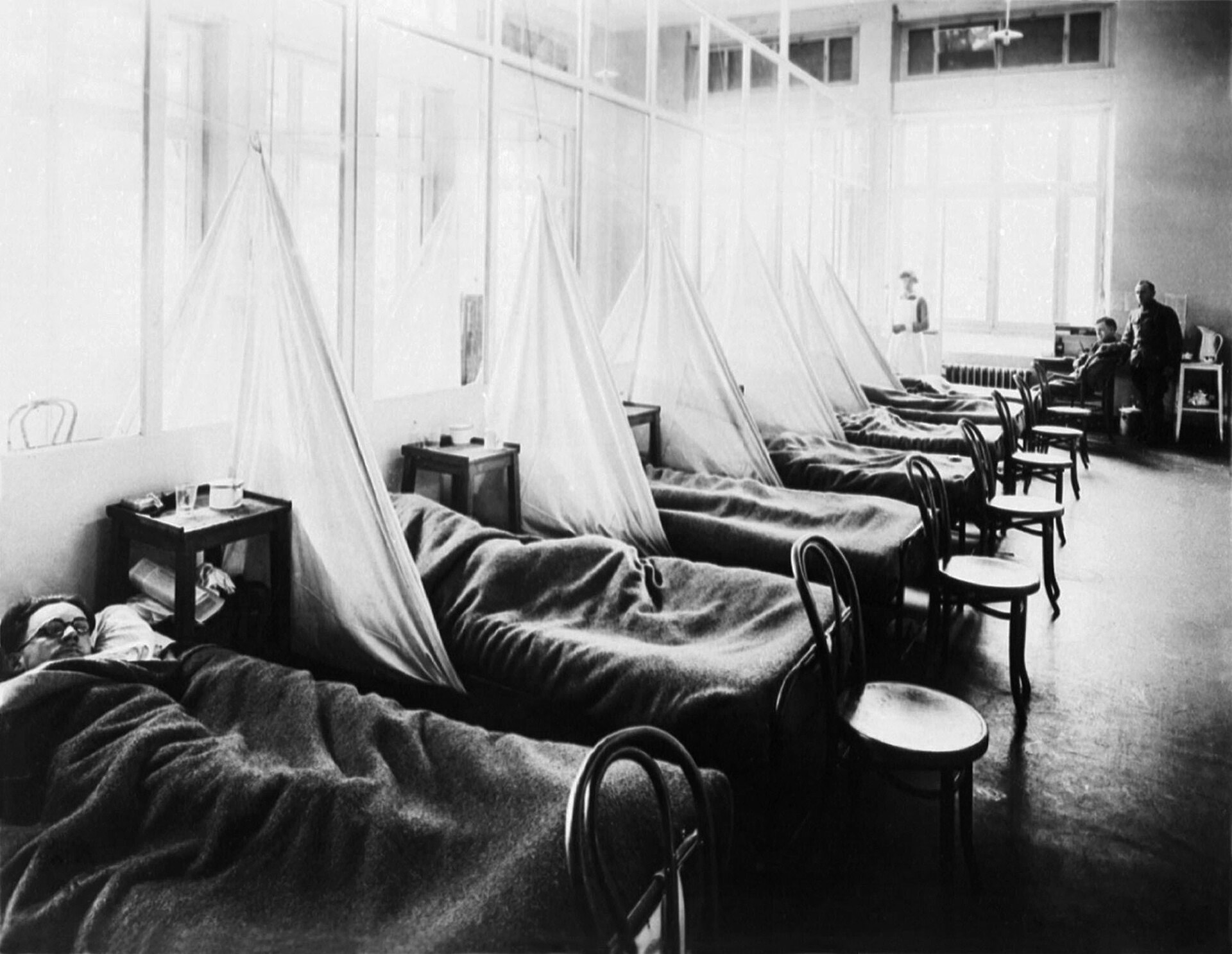 American Expeditionary Force flu patients at U.S. Army Camp Hospital no. 45 in Aix-les-Bains, France, 1918 Spanish satirical cartoon published in November 1918 depicting a "tragic game of football" between Mars, Greek god of war, and the Spanish Flu. There is a short poem as a caption which roughly translates to English as "Between flu and war, look at how they've left her, our poor Earth"  Mars, god of war, plays a "tragic game of football" with a skeleton personification of the Spanish flu, November 1918 The second wave began in the second half of August 1918, probably spreading to Boston, Massachusetts and Freetown, Sierra Leone, by ships from Brest, where it had likely arrived with American troops or French recruits for naval training.[99] From the Boston Navy Yard and Camp Devens (later renamed Fort Devens), about 30 miles west of Boston, other U.S. military sites were soon afflicted, as were troops being transported to Europe.[100] Helped by troop movements, it spread over the next two months to all of North America, and then to Central and South America, also reaching Brazil and the Caribbean on ships.[101] In July 1918, the Ottoman Empire saw its first cases in some soldiers.[102] From Freetown, the pandemic continued to spread through West Africa along the coast, rivers, and the colonial railways, and from railheads to more remote communities, while South Africa received it in September on ships bringing back members of the South African Native Labour Corps returning from France.[101] From there it spread around southern Africa and beyond the Zambezi, reaching Ethiopia in November.[103] On 15 September, New York City saw its first fatality from influenza.[104] The Philadelphia Liberty Loans Parade, held in Philadelphia, Pennsylvania, on 28 September 1918 to promote government bonds for World War I, resulted in 12,000 deaths after a major outbreak of the illness spread among people who had attended the parade.[105] From Europe, the second wave swept through Russia in a southwest–northeast diagonal front, as well as being brought to Arkhangelsk by the North Russia intervention, and then spread throughout Asia following the Russian Civil War and the Trans-Siberian railway, reaching Iran (where it spread through the holy city of Mashhad), and then later India in September, as well as China and Japan in October.[106] The celebrations of the Armistice of 11 November 1918 also caused outbreaks in Lima and Nairobi, but by December the wave was mostly over.[107] The second wave of the 1918 pandemic was much more deadly than the first. The first wave had resembled typical flu epidemics; those most at risk were the sick and elderly, while younger, healthier people recovered easily. October 1918 was the month with the highest fatality rate of the whole pandemic.[108] In the United States, ~292,000 deaths were reported between September–December 1918, compared to ~26,000 during the same time period in 1915.[97] The Netherlands reported over 40,000 deaths from influenza and acute respiratory disease. Bombay reported ~15,000 deaths in a population of 1.1 million.[109] The 1918 flu pandemic in India was especially deadly, with an estimated 12.5–20 million deaths in the last quarter of 1918 alone.[96][page needed] Third wave of 1919 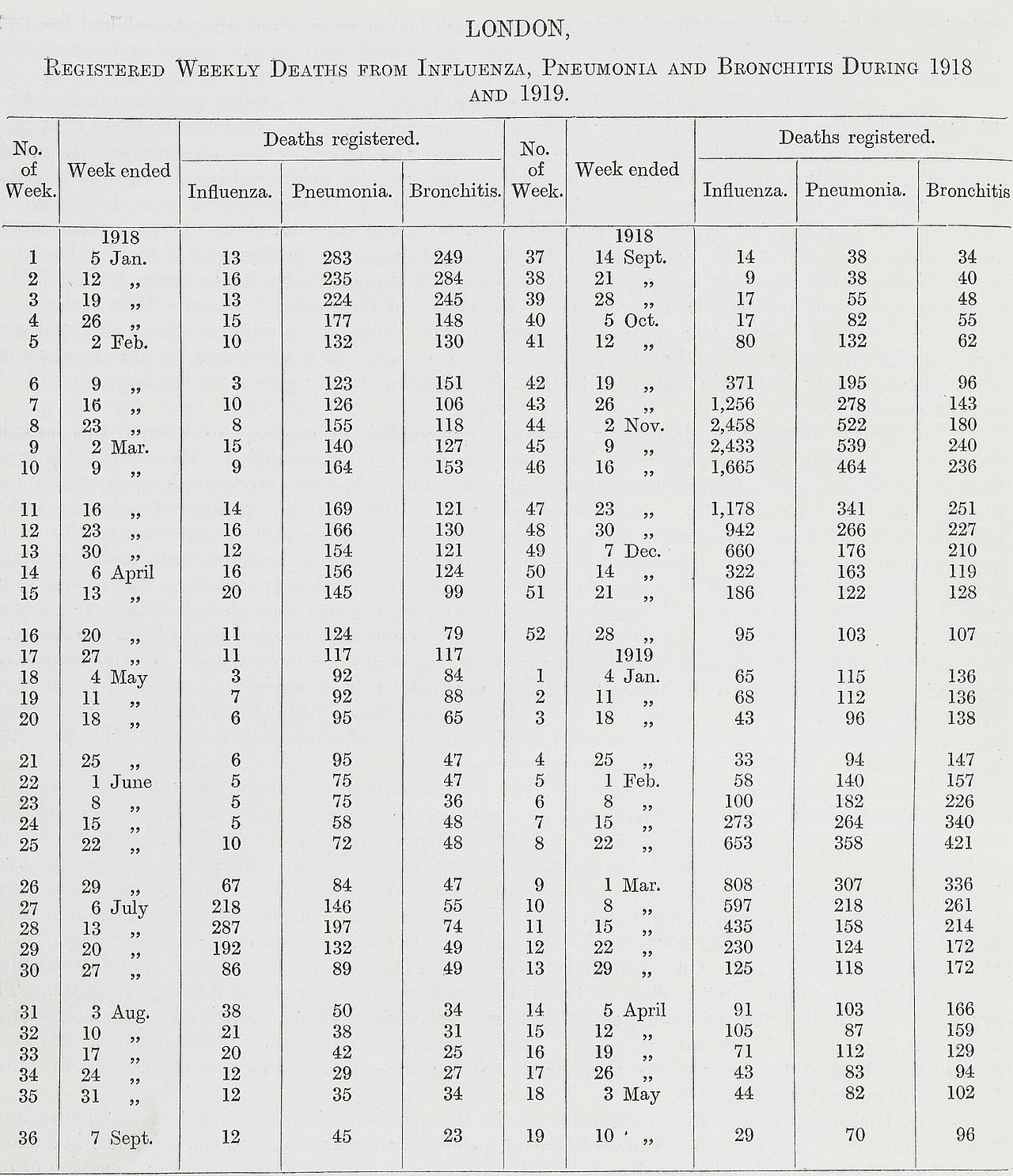 London weekly deaths from influenza during 1918 and 1919 Pandemic activity persisted, in general, into 1919 in many places. This persistence in activity is possibly attributable to climate, specifically in the Northern Hemisphere, where it was winter and thus the usual time for influenza activity.[110][111] The pandemic nonetheless continued into 1919 largely independent of region and climate.[110] Cases began to rise again in some parts of the United States as early as late November 1918,[112] with the Public Health Service issuing its first report of a "recrudescence of the disease" being felt in "widely scattered localities" in early December.[113] This resurgent activity varied across the country, however, possibly on account of differing restrictions.[111] Michigan, for example, experienced a swift resurgence of influenza that reached its peak in December, possibly as a result of the lifting of the ban on public gatherings.[114] Pandemic interventions, such as bans on public gatherings and the closing of schools, were reimposed in many places in an attempt to suppress the spread.[113] There was "a very sudden and very marked rise in general death rate" in most cities in January 1919; nearly all experienced "some degree of recrudescence" of the flu in January and February.[115]: 153–154 Significant outbreaks occurred in cities including Los Angeles,[116] New York City,[1] Memphis, Nashville, San Francisco, and St. Louis.[117] By 21 February, with some local variation, influenza activity was reported to have been declining since mid-January in all parts of the country.[118] Following this "first great epidemic period" that had commenced in October 1918, deaths from pneumonia and influenza were "somewhat below average" in the large cities of the United States between May 1919 and January 1920.[115]: 158 Nonetheless, nearly 160,000 deaths were attributed to these causes in the first six months of 1919.[119] It was not until later in the winter and into the spring that a clearer resurgence appeared in Europe. A significant third wave had developed in England and Wales by mid-February, peaking in early March, though it did not fully subside until May.[120] France also experienced a significant wave that peaked in February, alongside the Netherlands. Norway, Finland, and Switzerland saw recrudescences of pandemic activity in March, and Sweden in April.[121] Much of Spain was affected by "a substantial recrudescent wave" of influenza between January and April 1919.[122] Portugal experienced a resurgence in pandemic activity that lasted from March to September 1919, with the greatest impact being felt on the west coast and in the north of the country; all districts were affected between April and May specifically.[123] Influenza entered Australia for the first time in January 1919 after a strict maritime quarantine had shielded the country through the latter part of 1918.[124] It assumed epidemic proportions first in Melbourne, peaking in mid-February.[125] The flu soon appeared in neighboring New South Wales and South Australia and then spread across the country throughout the year.[124] New South Wales experienced its first wave of infection between mid-March and late May,[126] while a second, more severe wave occurred in Victoria between April and June.[125] Land quarantine measures hindered the spread of the disease, resulting in varied experiences of exposures and outbreaks among the various states. Queensland was not infected until late April; Western Australia avoided the disease until early June, and Tasmania remained free from it until mid-August.[124] Out of the six states, Victoria and New South Wales experienced generally more extensive epidemics. Each experienced another significant wave of illness over the winter. The second epidemic in New South Wales was more severe than the first,[126] while Victoria saw a third wave that was somewhat less extensive than its second, more akin to its first.[125] The disease also reached other parts of the world for the first time in 1919, such as Madagascar, which saw its first cases in April; the outbreak had spread to practically all sections of the island by June.[127] In other parts, influenza recurred in the form of a true "third wave". Hong Kong experienced another outbreak in June,[128] as did South Africa during its fall and winter months in the Southern Hemisphere.[129][130][131] New Zealand also experienced some cases in May.[132] Parts of South America experienced a resurgence of pandemic activity throughout 1919. A third wave hit Brazil between January and June.[110] Between July 1919 and February 1920, Chile, which had been affected for the first time just in October 1918, experienced a severe second wave, with mortality peaking in August 1919.[133] Montevideo similarly experienced a second outbreak between July and September.[134] The third wave particularly affected Spain, Serbia, Mexico and Great Britain, resulting in hundreds of thousands of deaths.[135] It was in general less severe than the second wave but still much more deadly than the initial first wave. Fourth wave of 1920  Public health recommendations from the Illustrated Current News In the Northern Hemisphere, fears of a "recurrence" of the flu grew as fall approached. Experts cited the history of past flu epidemics, such as that of 1889–1890, to predict that such a recurrence a year later was not unlikely,[136][137] though not all agreed.[138] In September 1919, U.S. Surgeon General Rupert Blue said a return of the flu later in the year would "probably, but by no means certainly," occur.[139] France had readied a public information campaign before the end of the summer,[140] and Britain began preparations in the autumn with the manufacture of vaccine.[141] In Japan, the flu broke out again in December and spread rapidly throughout the country, a fact attributed at the time to the coming of cold weather.[142][143] Pandemic-related measures were renewed to check the spread of the outbreak, and health authorities recommended the use of masks.[143] The epidemic intensified in the latter part of December before swiftly peaking in January.[144] Between October 1919 and 23 January 1920, 780,000 cases were reported across the country, with at least 20,000 deaths recorded by that date. This apparently reflected "a condition of severity three times greater than for the corresponding period of" 1918–1919, during Japan's first epidemic.[144] Nonetheless, the disease was regarded as being milder than it had been the year before, albeit more infectious.[145] Despite its rapid peak at the beginning of the year, the outbreak persisted throughout the winter, before subsiding in the spring.[146] In the United States, there were "almost continuously isolated or solitary cases" of flu throughout the spring and summer months of 1919.[147] An increase in scattered cases became apparent as early as September,[148] but Chicago experienced one of the first major outbreaks of the flu beginning in the middle of January.[149] The Public Health Service announced it would take steps to "localize the epidemic",[150] but the disease was already causing a simultaneous outbreak in Kansas City and quickly spread outward from the center of the country in no clear direction.[147] A few days after its first announcement, PHS issued another assuring that the disease was under the control of state health authorities and that an outbreak of epidemic proportions was not expected.[151] It became apparent within days of the start of Chicago's explosive growth in cases that the flu was spreading in the city at an even faster rate than in winter 1919, though fewer were dying.[152] Within a week, new cases in the city had surpassed its peak during the 1919 wave.[153] Around the same time, New York City began to see its own sudden increase in cases,[154] and other cities around the country were soon to follow.[155] Certain pandemic restrictions, such as the closing of schools and theaters and the staggering of business hours to avoid congestion, were reimposed in cities like Chicago,[156] Memphis,[157] and New York City.[158] As they had during the epidemic in fall 1918, schools in New York City remained open,[158] while those in Memphis were shuttered as part of more general restrictions on public gatherings.[157] 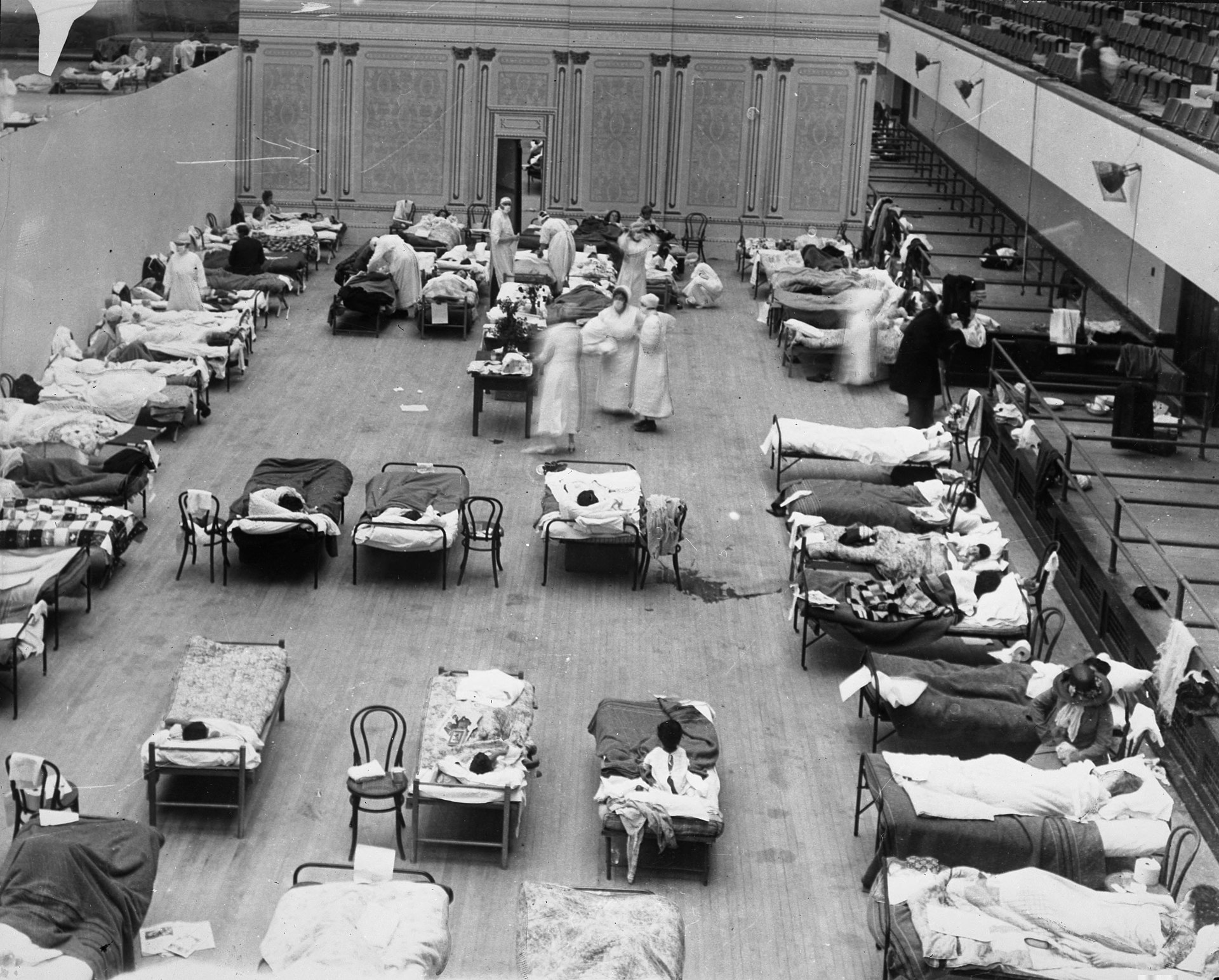 American Red Cross nurses tend to flu patients in temporary wards set up inside the Oakland Municipal Auditorium The fourth wave in the United States subsided as swiftly as it had appeared, reaching a peak in early February.[159] "An epidemic of considerable proportions marked the early months of 1920", the U.S. Mortality Statistics would later note; according to data at this time, the epidemic resulted in one third as many deaths as the 1918–1919 experience.[160] New York City alone reported 6,374 deaths between December 1919 and April 1920, almost twice the number of the first wave in spring 1918.[1] Other U.S. cities including Detroit, Milwaukee, Kansas City, Minneapolis, and St. Louis were hit particularly hard, with death rates higher than all of 1918.[117] The Territory of Hawaii experienced its peak of the pandemic in early 1920, recording 1,489 deaths from flu-related causes, compared with 615 in 1918 and 796 in 1919.[161] Poland experienced a devastating outbreak during the winter months, with its capital Warsaw reaching a peak of 158 deaths in a single week, compared to the peak of 92 reached in December 1918; however, the 1920 epidemic passed in a matter of weeks, while the 1918–1919 wave had developed over the entire second half of 1918.[162] By contrast, the outbreak in western Europe was considered "benign", with the age distribution of deaths beginning to take on that of seasonal flu.[163] Five countries in Europe (Spain, Denmark, Finland, Germany and Switzerland) recorded a late peak between January–April 1920.[121] Mexico experienced a fourth wave between February and March. In South America, Peru experienced "asynchronous recrudescent waves" throughout the year. A severe third wave hit Lima, the capital city, between January and March, resulting in an all-cause excess mortality rate approximately four times greater than that of the 1918–1919 wave. Ica similarly experienced another severe pandemic wave in 1920, between July and October.[164] A fourth wave also occurred in Brazil, in February.[110] Korea and Taiwan, both colonies of Japan at this time, also experienced pronounced outbreaks in late 1919 and early 1920.[165][166] Post-pandemic By mid-1920, the pandemic was largely considered to be "over" by the public as well as governments.[167] Though parts of Chile experienced a third, milder wave between November 1920 and March 1921,[133] the flu seemed to be mostly absent through the winter of 1920–1921.[115]: 167 In the United States, for example, deaths from pneumonia and influenza were "very much lower than for many years".[115]: 167 Seasonal Influenza after the end of the pandemic, began to be reported again from many places in 1921.[115]: 168 Influenza continued to be felt in Chile, where a post pandemic fourth wave affected seven of its 24 provinces between June and December 1921.[133] The winter of 1921–1922 was the first major reappearance of seasonal influenza in the Northern Hemisphere after the pandemic ended, in many parts its most significant occurrence since the main pandemic in late 1918. Northwestern Europe was particularly affected. All-cause mortality in the Netherlands approximately doubled in January 1922 alone.[115]: 168 In Helsinki, a major epidemic (the fifth since 1918) prevailed between November and December 1921.[168] The flu was also widespread in the United States, its prevalence in California reportedly greater in early March 1922 than at any point since the pandemic ended in 1920.[115]: 172 In the years after 1920, the disease, a novel one in 1918, assumed a more familiar nature, coming to represent at least one form of the "seasonal flu". The virus, H1N1, remained endemic, occasionally causing more severe or otherwise notable outbreaks as it gradually evolved over the years.[169] The period since its initial appearance in 1918 has been termed a "pandemic era", in which all flu pandemics since its emergence have been caused by its own descendants.[170] Following the first of these post-1918 pandemics, in 1957, the virus was totally displaced by the novel H2N2, the reassortant product of the human H1N1 and an avian influenza virus, which thereafter became the active influenza A virus in humans.[169] In 1977, an influenza virus bearing a very close resemblance to the seasonal H1N1, which had not been seen since the 1950s, appeared in Russia and subsequently initiated a "technical" pandemic that principally affected those 26 years of age and younger.[171][172] While some natural explanations, such as the virus remaining in some frozen state for 20 years,[172] have been proposed to explain this unprecedented[173] phenomenon, the nature of influenza itself has been cited in favor of human involvement of some kind, such as an accidental leak from a lab where the old virus had been preserved for research purposes.[172] Following this miniature pandemic, the reemerged H1N1 became endemic once again but did not displace the other active influenza A virus, H3N2 (which itself had displaced H2N2 through a pandemic in 1968).[171][169] For the first time, two influenza A viruses were observed in cocirculation.[174] This state of affairs has persisted even after 2009, when a novel H1N1 virus emerged, sparked a pandemic, and thereafter took the place of the seasonal H1N1 to circulate alongside H3N2.[174] Potential origins Despite its name, historical and epidemiological data cannot identify the geographic origin of the Spanish flu.[2] However, several theories have been proposed. United States The first confirmed cases originated in the United States. Historian Alfred W. Crosby stated in 2003 that the flu originated in Kansas,[175] and author John M. Barry described a January 1918 outbreak in Haskell County, Kansas, as the point of origin in his 2004 article.[81] A 2018 study of tissue slides and medical reports led by evolutionary biology professor Michael Worobey found evidence against the disease originating from Kansas, as those cases were milder and had fewer deaths compared to the infections in New York City in the same period. The study did find evidence through phylogenetic analyses that the virus likely had a North American origin, though it was not conclusive. In addition, the haemagglutinin glycoproteins of the virus suggest that it originated long before 1918, and other studies suggest that the reassortment of the H1N1 virus likely occurred in or around 1915.[176] Europe  Edvard Munch (1863–1944), Self-Portrait with the Spanish Flu (1919)  Egon Schiele (1890–1918), Die Familie, painted a few days before his death and just after the death of his wife Edith from the Spanish flu[177] The major U.K. troop staging and hospital camp in Étaples in France has been theorized by virologist John Oxford as being at the center of the Spanish flu.[178] His study found that in late 1916 the Étaples camp was hit by the onset of a new disease with high mortality that caused symptoms similar to the flu.[179][178] According to Oxford, a similar outbreak occurred in March 1917 at army barracks in Aldershot,[180] and military pathologists later recognized these early outbreaks as the same disease as the Spanish flu.[181][178] The overcrowded camp and hospital at Étaples was an ideal environment for the spread of a respiratory virus. The hospital treated thousands of victims of poison gas attacks, and other casualties of war, and 100,000 soldiers passed through the camp every day. It also was home to a piggery and poultry was regularly brought in from surrounding villages to feed the camp. Oxford and his team postulated that a precursor virus, harbored in birds, mutated and then migrated to pigs kept near the front.[180][181] A report published in 2016 in the Journal of the Chinese Medical Association found evidence that the 1918 virus had been circulating in the European armies for months and possibly years before the 1918 pandemic.[182] Political scientist Andrew Price-Smith published data from the Austrian archives suggesting the influenza began in Austria in early 1917.[183] A 2009 study in Influenza and Other Respiratory Viruses found that Spanish flu mortality simultaneously peaked within the two-month period of October and November 1918 in all fourteen European countries analyzed, which is inconsistent with the pattern that researchers would expect if the virus had originated somewhere in Europe and then spread outwards.[121] China In 1993, Claude Hannoun, the leading expert on the Spanish flu at the Pasteur Institute, asserted the precursor virus was likely to have come from China and then mutated in the United States near Boston and from there spread to Brest, France, Europe's battlefields, the rest of Europe, and the rest of the world, with Allied soldiers and sailors as the main disseminators.[184] Hannoun considered several alternative hypotheses of origin, such as Spain, Kansas, and Brest, as being possible, but not likely.[184] In 2014, historian Mark Humphries argued that the mobilization of 96,000 Chinese laborers to work behind the British and French lines might have been the source of the pandemic. Humphries, of the Memorial University of Newfoundland in St. John's, based his conclusions on newly unearthed records. He found archival evidence that a respiratory illness that struck northern China (where the laborers came from) in November 1917 was identified a year later by Chinese health officials as identical to the Spanish flu.[185][186] Unfortunately, no tissue samples have survived for modern comparison.[187] Nevertheless, there were some reports of respiratory illness on parts of the path the laborers took to get to Europe, which also passed through North America.[187] China was one of the few regions of the world seemingly less affected by the Spanish flu pandemic, where several studies have documented a comparatively mild flu season in 1918.[188][189][190] (Although this is disputed due to lack of data during the Warlord Period, see Around the globe.) This has led to speculation that the Spanish flu pandemic originated in China,[190][191] as the lower rates of flu mortality may be explained by the Chinese population's previously acquired immunity to the flu virus.[174][190] In the Guangdong Province it was reported that early outbreaks of influenza in 1918 disproportionately impacted young men. The June outbreak infected children and adolescents between 11 and 20 years of age, while the October outbreak was most common in those aged 11 to 15.[192] A report published in 2016 in the Journal of the Chinese Medical Association found no evidence that the 1918 virus was imported to Europe via Chinese and Southeast Asian soldiers and workers and instead found evidence of its circulation in Europe before the pandemic.[182] The 2016 study found that the low flu mortality rate (an estimated one in a thousand) recorded among the Chinese and Southeast Asian workers in Europe suggests that the Asian units were not different from other Allied military units in France at the end of 1918 and, thus, were not a likely source of a new lethal virus.[182] Further evidence against the disease being spread by Chinese workers was that workers entered Europe through other routes that did not result in a detectable spread, making them unlikely to have been the original hosts.[176] |
歴史 年表 1918年初頭の最初の波  スペイン風邪のパンデミック時にアメリカ赤十字社から支給された布製マスクを着用したシアトルの警察官、1918年12月 パンデミックは、それ以前にも患者はいたものの、1918年3月4日にカンザス州のキャンプ・ファンストンの軍用炊事係アルバート・ギッチェルの症例が記 録されたことから始まったとされている。[89] しかし、この病気は1918年1月には早くも200マイル(320キロ)離れたハスケル郡でも確認されており、地元の医師ローリング・マイナーは 米国公衆衛生局の学術誌『Public Health Reports』の編集者に警告を発した。[81] 3月4日にキャンプ・ファンストンで最初の症例が確認されてから数日のうちに、キャンプの522人の兵士が体調不良を訴えた。[90] 1918年3月11日までに、ウイルスはニューヨーク州クイーンズにまで到達した。[91] 3月と4月に予防措置を取らなかったことは、後に批判された。[92] 米国が第一次世界大戦に参戦すると、この病気は、アメリカ遠征軍の主要な訓練場であるキャンプ・ファンストンから、他の米国陸軍のキャンプやヨーロッパへ と急速に広がり、1918年4月までに米国中西部、東海岸、フランスの港で流行となり、 。その後、急速にフランス、イギリス、イタリア、スペインの他の地域にも広がり、5月にはヴロツワフとオデッサに到達した。[89] ブレスト・リトフスク条約(1918年3月)の締結後、ドイツはロシア人捕虜の解放を開始し、解放された捕虜が その病気は自国にも持ち込まれた。[93] 5月には北アフリカ、インド、日本に到達し、4月には東南アジアでの感染例が記録されていることから、その後まもなく世界中に広がった可能性が高い。 [94] 6月には中国での発生が報告された。[95] 7月にオーストラリアに到達した後、流行は収まり始めた。[94] インフルエンザの最初の流行は1918年第1四半期から始まり、比較的軽症であった。死亡率は通常より著しく高いということはなく、米国では1918年の 最初の6か月間で約7万5千人のインフルエンザ関連死が報告されたが、 1915年の同時期には約3,000人の死者が出ていた。[97] スペインのマドリードでは、1918年5月から6月にかけてインフルエンザによる死亡者は1,000人以下であった。[98] 1918年第1四半期には隔離の報告はなかった。しかし、第一次波は第一次世界大戦の軍事作戦に大きな混乱をもたらし、フランス軍の4分の3、イギリス軍 の半数、そして90万人以上のドイツ兵が感染した。 1918年後半の致命的な第二次波  1918年、フランス、エグ・レ・バンの米陸軍第45野戦病院のアメリカ遠征軍のインフルエンザ患者 1918年11月に発表されたスペイン風刺漫画。ギリシャ神話の戦争の神マルスとスペイン風邪による「悲劇的なサッカーの試合」を描いている。キャプショ ンには短い詩が添えられており、英語に訳すと「インフルエンザと戦争の間、地球がどれほどひどい状態になっているか見てみろ」となる  戦争の神マルスがスペイン風邪の骸骨と「悲劇的なサッカーの試合」をしている。1918年11月 1918年8月後半に第2波が始まり、おそらくブレストからボストン、マサチューセッツ州、フリータウン、シエラレオネに、アメリカ軍または海軍訓練のた めのフランス人志願兵とともに到着した船舶によって広がった。[99] ボストン海軍造船所とキャンプ・デベンズ(後にフォート・デベンズと改名)から、ボストンから西に約30マイル離れた他の米軍 軍事施設も被害を受け、ヨーロッパに輸送される部隊も被害を受けた。[100] 軍の移動により、このウイルスは2か月間で北米全土に広がり、その後は中央アメリカと南アメリカにも広がった。ブラジルとカリブ海地域にも船舶を通じて到 達した。[101] 1918年7月、オスマン帝国では兵士の一部に最初の症例が見られた。[102] フリータウンから、西アフリカの沿岸部、河川、植民地鉄道に沿ってパンデミックは拡大し、鉄道の終着駅からさらに離れた地域にも広がった。一方、南アフリ カでは、9月にフランスから帰還した南アフリカ先住民労働部隊の兵士を乗せた船によって、ウイルスが持ち込まれた。[101] そこからウイルスはアフリカ南部に広がり、11月にはザンベジ川を越えてエチオピアに到達した。[103] 9月15日、ニューヨーク市でインフルエンザによる初の死者が出た。[104] 1918年9月28日にペンシルベニア州フィラデルフィアで開催された第一次世界大戦のための公債を促進するためのフィラデルフィア・リバティー・ロー ン・パレードでは、パレードに参加した人々の間でインフルエンザが大流行し、12,000人が死亡した。[105] ヨーロッパから始まった第二波は、ロシアを南西から北東に向かう対角線状に襲い、北ロシア介入によってアルハンゲリスクにも到達した。その後、ロシア内戦 とシベリア横断鉄道に沿ってアジア全域に広がり、イラン(聖地マシュハドに広がった)に到達し、 マシュハドの聖地に広がった)後、9月にはインド、10月には中国と日本にも広がった。[106] 1918年11月11日の休戦協定の祝賀会もリマとナイロビでの発生の原因となったが、12月にはその流行はほぼ終息した。[107] 1918年のパンデミックの第2波は、第1波よりもはるかに致死率が高かった。第1波は典型的なインフルエンザの流行に似ており、最もリスクが高いのは病 人や高齢者で、若く健康な人々は容易に回復した。1918年10月は、パンデミック全体で最も死亡率が高かった月であった。[108] 米国では、1918年9月から12月の間に約29万2000人の死亡が報告されたが、1915年の同じ時期では約2万6000人であった。[97] オランダでは、インフルエンザと急性呼吸器疾患による死亡が4万人を超えたと報告された。ボンベイでは、人口110万人のうち約1万5000人が死亡した と報告されている。[109] インドにおける1918年のインフルエンザのパンデミックは特に致命的であり、1918年の最後の四半期だけで推定1250万~2000万人が死亡した。 [96][要出典] 1919年の第3波  1918年から1919年のロンドンにおけるインフルエンザによる週ごとの死亡者数 パンデミックの活動は、多くの場所で概ね1919年まで続いた。この活動の持続は、おそらく気候、特に北半球の冬の時期で、インフルエンザの活動が活発に なる時期であったことによるものと考えられる。[110][111] しかし、パンデミックは地域や気候とはほとんど関係なく1919年も続いた。[110] 1918年11月下旬には早くも、米国の一部地域で再び患者数が増加し始め[112]、12月初旬には「広範囲にわたる地域」で「病気の再流行」が感じら れるという公衆衛生局による最初の報告書が発表された[113]。しかし、この再流行は国によって異なり、おそらくは 。ミシガン州では、おそらく集会禁止令が解除されたことが原因で、12月にインフルエンザが急速に再流行し、ピークに達した。[114] パンデミック対策として、集会禁止令や学校閉鎖が多くの地域で再び実施され、感染拡大の抑制が試みられた。[113] 1919年1月には、ほとんどの都市で「死亡率が非常に急激かつ顕著に上昇」し、1月と2月にはほぼすべての都市でインフルエンザの「ある程度の再流行」 が見られた。[115]:153–154 ロサンゼルス、[116] ニューヨーク市、[ 1] メンフィス、ナッシュビル、サンフランシスコ、セントルイスでも発生した。[117] 2月21日までに、地域差はあるものの、1月中旬以降、全米各地でインフルエンザの活動が減少していることが報告された。[118] 1918年10月に始まったこの「最初の大きな流行期」の後、 1919年5月から1920年1月までの間、米国の大都市における肺炎およびインフルエンザによる死亡者数は「平均よりやや下回る程度」であった。 [115]:158 それにもかかわらず、1919年の最初の6か月間で、これらの原因による死亡者数は16万人近くに上った。[119] ヨーロッパで明確な回復傾向が見られるようになったのは、冬が終わり春を迎えてからであった。2月中旬にはイングランドとウェールズで第3の大きな波が発 生し、3月初旬にピークに達したが、完全に沈静化するのは5月になってからであった。[120] フランスでもオランダと同様に、2月に大きな波が発生した。ノルウェー、フィンランド、スイスでは3月に、スウェーデンでは4月にパンデミックの再流行が 見られた。[121] スペインの大部分は、1919年1月から4月にかけて「大幅な再流行の波」に襲われた。[122] ポルトガルでは、1919年3月から9月にかけてパンデミックの活動が再燃し、その影響は西海岸と北部で最も大きかった。特に4月から5月にかけては、す べての地域で影響が見られた。[123] 厳格な海上検疫により1918年後半のオーストラリアは守られていたが、1919年1月に初めてインフルエンザがオーストラリアに上陸した。[124] メルボルンで最初に流行し、2月中旬にピークに達した。[125] インフルエンザはすぐに 隣接するニュー・サウス・ウェールズ州と南オーストラリア州にもすぐに広がり、その後、1年を通じて全国に広がった。[124] ニュー・サウス・ウェールズ州では3月中旬から5月下旬にかけて最初の感染の波が起こり、[126] ビクトリア州では4月から6月にかけて2度目の、より深刻な感染の波が起こった。[125] 検疫措置により感染の拡大は妨げられ、州によって感染や流行の状況は様々であった。クイーンズランド州では4月下旬まで感染が確認されず、西オーストラリ ア州では6月初旬まで、タスマニア州では8月中旬まで感染が確認されなかった。6つの州のうち、ビクトリア州とニューサウスウェールズ州では、より広範囲 にわたる流行が確認された。冬には、それぞれにさらに大きな流行の波が到来した。ニューサウスウェールズ州では2度目の流行が1度目よりも深刻であった が、ビクトリア州では3度目の流行は2度目よりも規模が小さく、1度目により似たものとなった。 1919年には、マダガスカルなど、初めて世界中の他の地域にも感染が拡大した。同国では4月に最初の感染者が確認され、6月にはほぼ全土に広がった。 [127] その他の地域では、インフルエンザが「第3波」として再び発生した。香港では6月に新たな流行が発生し[128]、南半球の南アフリカでも秋から冬にかけ て流行した[129][130][131]。ニュージーランドでも5月にいくつかの症例が確認された[132]。 南米の一部地域では、1919年を通してパンデミックの活動が再燃した。第3波は1月から6月にかけてブラジルを襲った。[110] 1919年7月から1920年2月にかけて、1918年10月に初めて感染が確認されたチリでは、1919年8月に死亡率がピークに達する深刻な第2波が 発生した。[133] モンテビデオでも同様に、7月から9月にかけて第2の流行が発生した。[134] 第3波は特にスペイン、セルビア、メキシコ、イギリスに大きな影響を与え、数十万人の死者を出した。[135] 第2波ほど深刻ではなかったが、それでも第1波の最初の感染拡大よりもはるかに多くの死者を出した。 1920年の第4波  イラストレイテッド・カレント・ニュースによる公衆衛生勧告 北半球では、秋が近づくにつれ、インフルエンザの「再流行」への懸念が高まった。専門家は、1889年から1890年にかけての流行など過去のインフルエ ンザの流行の歴史を挙げ、1年後の再流行の可能性は低くないと予測したが、全員が同意したわけではなかった。1919年9月、米国の 米国公衆衛生局長官ルパート・ブルーは、その年の後半にインフルエンザが再流行する可能性は「おそらく、しかし確実に」あると述べた。[139] フランスは夏が終わる前に広報キャンペーンの準備を整え[140]、イギリスは秋にワクチン製造の準備を開始した。[141] 日本では12月に再びインフルエンザが流行し、急速に全国に広がった。この事実は、当時、寒さが到来したことによるものとされた。[142][143] パンデミック関連の対策が再び実施され、流行の拡大を食い止めるため、保健当局はマスクの使用を推奨した。[143] 12月後半に流行が激化し、1月に急速にピークに達した。[144] 1919年10月から1920年1月23日までの間に、全国で780,000件の症例が報告され、少なくとも20,000人の死亡が記録された。これは、 日本における最初の流行の1918年から1919年の同時期と比較して「3倍の深刻な状況」を反映しているように思われた。[144] それでも、この病気は、感染力は強かったものの、前年よりも症状は軽いとみなされていた。[145] 年初めに急速にピークに達したものの、流行は冬の間中続き、春になってようやく沈静化した。[146] 米国では、1919年の春から夏にかけて「ほぼ絶え間なく」インフルエンザの「孤立した、あるいは単独の症例」が報告された。[147] 9月には早くも散発的な症例の増加が明らかになったが、[148] シカゴでは1月半ばからインフルエンザの最初の大きな流行のひとつが発生した。[149] 公衆衛生局は「 「流行を局所化する」ための措置を取ると発表したが[150]、この病気はすでにカンザスシティで同時多発的な発生を引き起こしており、その後は明確な方 向性もなく、米国の中心部から急速に広がっていった。[147] 最初の発表から数日後、PHSは再度、この病気は州の保健当局の管理下にあり、流行規模の発生は予想されないという確約を発表した。[151] シカゴでの感染が爆発的に増加し始めた数日後には、1919年の冬よりもさらに速いペースでインフルエンザが蔓延していることが明らかになったが、死亡者 数は少なかった。[152] 1週間も経たないうちに、シカゴでの新たな感染者数は1919年の流行時のピークを上回った。[ 153] ほぼ同時期に、ニューヨーク市でも急激な感染者数の増加が見られ始め[154]、やがて全米の他の都市でも同様の事態となった[155]。学校や劇場を閉 鎖し、混雑を避けるために営業時間をずらすなど、パンデミック対策として実施されていた一定の制限が、 シカゴ[156]、メンフィス[157]、ニューヨーク市[158]などでは、学校や劇場を閉鎖し、混雑を避けるために営業時間をずらすといったパンデ ミック対策が再び実施された。  オークランド市公会堂内に設置された臨時病棟で、アメリカ赤十字社の看護師がインフルエンザ患者の看護にあたる 米国における第4の流行は、発生から急速に沈静化し、2月初旬にピークに達した。[159] 米国死亡率統計は後に、「1920年の初期には、相当な規模の流行がみられた」と記している。この時期のデータによると、この流行による死亡者数は、 1918年から1919年の流行による死亡者数の3分の1であった 。ニューヨーク市だけで1919年12月から1920年4月までの間に6,374人の死亡が報告され、1918年春の最初の流行のほぼ2倍に上った。 [1] デトロイト、ミルウォーキー、カンザスシティ、ミネアポリス、セントルイスを含む他の米国の都市は特に大きな打撃を受け 死亡率は1918年全体よりも高かった。[117] ハワイ準州では1920年初頭にパンデミックのピークを迎え、インフルエンザ関連死は1,489人に達した。1918年には615人、1919年には 796人が死亡している。[161] ポーランドでは冬の間に壊滅的な流行が発生し、首都ワルシャワでは1918年12月の92人のピークと比較して、1週間で158人の死者が出るピークに達 した。しかし、1920年の流行は数週間で終息したのに対し、1918年から1919年の流行は 1918年の後半全体にわたって広がっていた。[162] これとは対照的に、西ヨーロッパでの流行は「穏やか」で、死亡者の年齢分布は季節性インフルエンザのそれと似ていた。[163] ヨーロッパの5か国(スペイン、デンマーク、フィンランド、ドイツ、スイス)では、1920年1月から4月の間に後期のピークが記録された。[121] メキシコでは2月から3月にかけて第4波が発生した。南米ではペルーで「非同期再流行波」が1年を通じて発生した。1月から3月にかけてはリマ(首都)に 深刻な第3波が襲来し、あらゆる原因による死亡率は1918年から1919年の波の約4倍に達した。イカでも同様に、1920年の7月から10月にかけ て、別の深刻なパンデミックの波が到来した。[164] ブラジルでは2月に第4の波が発生した。[110] 当時日本の植民地であった韓国と台湾でも、1919年後半から1920年前半にかけて、顕著な流行が発生した。[165][166] パンデミック後 1920年半ばには、パンデミックは一般市民だけでなく政府も「終息した」とほぼ認識していた。[167] チリの一部では1920年11月から1921年3月にかけて3度目の、より穏やかな流行がみられたが、[133] 1920年から1921年の冬の間は、ほとんど流行しなかったようである。[115]:167 米国では、例えば、肺炎とインフルエンザによる死亡者数は「ここ何年もの間と比較して非常に少なかった」[115]:167 パンデミックの終息後、季節性インフルエンザは1921年から各地で再び報告され始めた。[115]:168 チリではパンデミック後の第4波が1921年6月から12月の間に24州のうち7州に影響を与えた。。1921年から1922年の冬は、パンデミック終息 後の北半球における季節性インフルエンザの最初の大きな再流行となり、多くの地域で1918年後半のパンデミック以来最も深刻な事態となった。特に北西 ヨーロッパが大きな影響を受けた。オランダでは、1922年1月だけで全死因による死亡率が約2倍に増加した。[115]: 168 ヘルシンキでは、1918年以来5度目となる大流行が1921年11月から12月にかけて発生した 。[168] インフルエンザは米国でも流行し、1922年3月初旬にはカリフォルニア州での感染率が1920年のパンデミック以来最も高くなったと報告されている。 [115]: 172 1920年以降、1918年に新型であったこの病気は、より身近な存在となり、少なくとも「季節性インフルエンザ」の一形態を代表するようになった。 H1N1型ウイルスはその後も流行を続け、時折、より深刻な、あるいは注目に値する流行を引き起こしながら、徐々に変異していった。[169] 1918年の初登場以来のこの期間は「パンデミック時代」と呼ばれ、それ以降のインフルエンザ・パンデミックはすべて、このウイルスの子孫によって引き起 こされている。[17 1918年以降の最初のパンデミックの後、1957年には、ヒトのH1N1と鳥インフルエンザウイルスの再集合体である新型H2N2が完全に主流となり、 その後、新型H2N2はヒトの間で活発なインフルエンザAウイルスとなった。 1977年には、1950年代以来目撃されていなかった季節性H1N1と非常に類似したインフルエンザウイルスがロシアで出現し、その後、主に26歳以下 の年齢層に影響を与えた「技術的」パンデミックが始まった。[171][172] ウイルスが20年間凍結状態のままであったというような、いくつかの自然現象による説明が提案されているが、[172] この前例のない現象[173] を説明するために、いくつかの自然現象が提案されているが、インフルエンザの性質そのものが、研究目的で古いウイルスを保存していた研究所からの偶発的な 漏出など、何らかの人為的な関与を支持する根拠として挙げられている。[172] このミニパンデミックの後、再出現したH1N1は再び常在化したが、他の活動中のインフルエンザAウイルスであるH3N2(これは1968年のパンデミッ クでH2N 1968年のパンデミックによりH2N2を駆逐した)H3N2が主流となった。[171][169] 初めて、2種類のインフルエンザAウイルスが同時に存在する状態が観察された。[174] この状態は、新型H1N1ウイルスが現れ、パンデミックを引き起こし、その後季節性H1N1に取って代わり、H3N2とともに流行した2009年以降も続 いている。[174] 起源の可能性 その名称にもかかわらず、歴史的および疫学的なデータではスペイン風邪の地理的な起源を特定することはできない。[2] しかし、いくつかの説が提唱されている。 米国 最初の確認された症例は米国で発生した。歴史学者のアルフレッド・W・クロスビーは2003年に、インフルエンザはカンザス州で発生したと述べている [175]。また、作家のジョン・M・バリーは、2004年の論文で、1918年1月にカンザス州ハスケル郡で発生したアウトブレイクを発生源として説明 している[81]。 2018年、進化生物学教授マイケル・ウォロベイが主導した組織スライドと医療報告書の研究では、カンザス州が発症地であるという証拠は見つからなかっ た。その理由は、同時期のニューヨーク市の感染症と比較すると、カンザス州での症例は症状が軽く、死亡者も少なかったからである。この研究では、系統発生 学分析により、ウイルスが北米で発生した可能性が高いという証拠は発見されたが、決定的なものではなかった。さらに、ウイルスのヘマグルチニン糖タンパク 質は、1918年よりもずっと以前に起源があったことを示唆しており、他の研究では、H1N1ウイルスの再集合は1915年頃に起こった可能性が高いこと が示唆されている。[176] ヨーロッパ  エドヴァルド・ムンク(1863年-1944年)『スペイン風邪とともに自画像』(1919年)  エゴン・シーレ(1890年-1918年)は、スペイン風邪で妻のエディトが死亡した直後に、死の数日前の『家族』を描いた。 フランス、エタプルにあったイギリス軍の主要な兵站基地および病院キャンプが、スペイン風邪の中心地であったという説がウイルス学者ジョン・オックス フォードによって提唱されている。[178] 彼の研究によると、1916年後半にエタプルキャンプが、インフルエンザに似た症状を引き起こす死亡率の高い新しい病気の発生に襲われたことが分かった。 [179][ オックスフォードによると、同様の集団発生は1917年3月にアルダショットの陸軍兵舎でも発生しており[180]、軍の病理学者は後にこれらの初期の集 団発生をスペイン風邪と同じ病気であると認識した[181][178]。エタプルの過密な収容所と病院は、呼吸器ウイルスの蔓延に理想的な環境であった。 病院では数千人の毒ガス攻撃の犠牲者やその他の戦争の犠牲者が治療を受け、毎日10万人の兵士が収容所を通過した。また、養豚場もあり、収容所の食料とし て、周辺の村から定期的に家禽が持ち込まれていた。オックスフォードと彼のチームは、鳥類に宿る前駆体ウイルスが変異し、戦線近くで飼育されている豚に移 動したと仮定した。[180][181] 2016年に『中国医学協会誌』で発表された報告書では、1918年のパンデミックの数ヶ月、あるいは数年前から、1918年のウイルスがヨーロッパの軍 隊で流行していた証拠が発見されたと報告している。[182] 政治学者のアンドリュー・プライス=スミスは、オーストリアの公文書館のデータから、インフルエンザは1917年初頭にオーストリアで始まった可能性を示 唆している。[183] 2009年の『インフルエンザおよびその他の呼吸器ウイルス』誌に掲載された研究では、分析対象となったヨーロッパの14か国すべてにおいて、1918年 10月と11月の2か月間にスペイン風邪による死亡率が同時にピークに達していたことが判明した。これは、ウイルスがヨーロッパのどこかで発生し、その 後、外部に広がっていったとすれば、研究者が予想するパターンと一致しない。 中国 1993年、パスツール研究所のスペイン風邪研究の第一人者であるクロード・ハヌーンは、前駆体ウイルスは中国からやって来て、米国ボストン近郊で変異 し、そこからフランスのブレスト、ヨーロッパの戦場 、連合軍の兵士や船員が主な感染者となり、ヨーロッパの戦場、ヨーロッパのその他の地域、そして世界のその他の地域へと広がっていったと主張した。 [184] ハヌンは、スペイン、カンザス、ブレストなど、いくつかの起源に関する代替仮説を可能性はあるが、可能性は低いとみなした。[184] 2014年、歴史家のマーク・ハンフリーズは、9万6000人の中国人労働者が英仏軍の後方で働くために動員されたことが、パンデミックの源となった可能 性があると主張した。ハンフリーズは、セントジョンズにあるニューファンドランド記念大学の教授であり、その結論は新たに発見された記録に基づいている。 彼は、1917年11月に中国北部(出稼ぎ労働者の出身地)を襲った呼吸器疾患が、1年後に中国の保健当局によってスペイン風邪と同一のものと特定された という記録を発見した。[185][186] 残念ながら、現代のものと比較できる組織サンプルは残っていない。[187] それでも、出稼ぎ労働者がヨーロッパに向かう際に通った航路の一部では呼吸器疾患の報告があり、その航路は北米も通っていた。[187] 中国は、スペイン風邪の世界的大流行の影響が比較的少なかった数少ない地域のひとつであり、複数の研究が1918年のインフルエンザの流行は比較的軽度で あったことを記録している。(ただし、軍閥時代に関するデータの不足により、この点については異論もある。世界全体を参照のこと。) このため、スペイン風邪のパンデミックは中国で発生したのではないかという推測がなされている。[190][191] インフルエンザによる死亡率が低かったのは、中国人口が以前にインフルエンザウイルスに対する免疫を獲得していたためである可能性がある。[174] [190] 広東省では、1918年のインフルエンザの初期の流行は若い男性に不均衡な影響を与えたと報告されている。6月の流行では11歳から20歳までの子供や若 者が感染し、10月の流行では11歳から15歳までの年齢層に最も多く見られた。[192] 2016年に『中国医学協会誌』で発表された報告書では、1918年のウイルスが中国人および東南アジアの兵士や労働者によってヨーロッパに持ち込まれた という証拠は見つからず、むしろ、パンデミック以前にヨーロッパでウイルスが循環していた証拠が見つかった。2016年の研究では、ヨーロッパで中国人お よび東南アジアの労働者たちに記録されたインフルエンザの死亡率の低さ(推定で1000人に1人)から、 1918年末のフランスにおける他の連合軍部隊とアジア部隊に違いは見られず、したがって、アジア部隊が新型の致死性ウイルスの感染源である可能性は低い ことを示唆している。[182] 中国人労働者によって新型ウイルスが蔓延したという説に反するさらなる証拠として、労働者は他のルートでヨーロッパに入国しており、そのルートではウイル スが蔓延した形跡は見られなかったため、彼らが最初の感染者である可能性は低い。[176] |
| Epidemiology and pathology Transmission and mutation 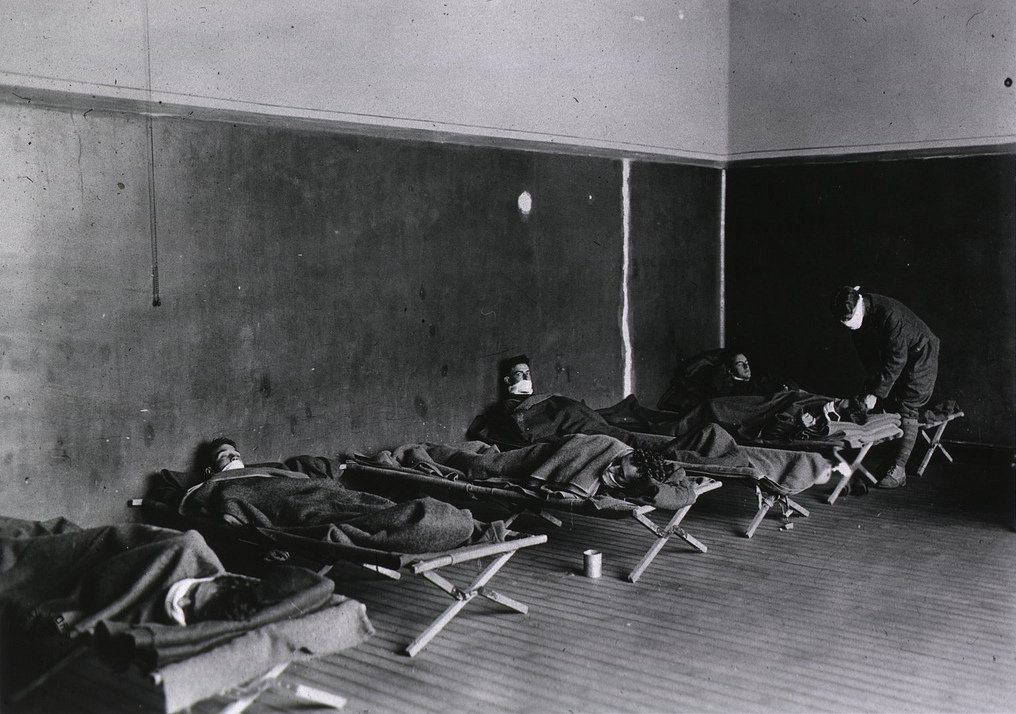 U.S. Army flu patients at Field Hospital No. 29 near Hollerich, Luxembourg 1918. As U.S. troops deployed en masse for the war effort in Europe, they carried the Spanish flu with them. The basic reproduction number of the virus was between 2 and 3.[193] The close quarters and massive troop movements of World War I hastened the pandemic, and probably both increased transmission and augmented mutation. The war may also have reduced people's resistance to the virus. Some speculate the soldiers' immune systems were weakened by malnourishment, as well as the stresses of combat and chemical attacks, increasing their susceptibility.[194][195] A large factor in the worldwide occurrence of the flu was increased travel. Modern transportation systems made it easier for soldiers, sailors, and civilian travelers to spread the disease.[196] Another was lies and denial by governments, leaving the population ill-prepared to handle the outbreaks.[197] The severity of the second wave has been attributed to the circumstances of the First World War.[198] In civilian life, natural selection favors a mild strain. Those who get very ill stay home, and those mildly ill continue with their lives, preferentially spreading the mild strain. In the trenches, natural selection was reversed. Soldiers with a mild strain stayed where they were, while the severely ill were sent on crowded trains to crowded field hospitals, spreading the deadlier virus. The second wave began, and the flu quickly spread around the world again. Consequently, during modern pandemics, health officials look for deadlier strains of a virus when it reaches places with social upheaval.[199] The fact that most of those who recovered from first-wave infections had become immune showed that it must have been the same strain of flu. This was most dramatically illustrated in Copenhagen, which escaped with a combined mortality rate of just 0.29% (0.02% in the first wave and 0.27% in the second wave) because of exposure to the less-lethal first wave.[200] For the rest of the population, the second wave was far more deadly; the most vulnerable people were those like the soldiers in the trenches – adults who were young and fit.[201] After the lethal second wave struck in late 1918, new cases dropped abruptly. In Philadelphia, for example, 4,597 people died in the week ending 16 October, but by 11 November, influenza had almost disappeared from the city. One explanation for the rapid decline in the lethality of the disease is that doctors became more effective in the prevention and treatment of pneumonia that developed after the victims had contracted the virus. However, John Barry stated in his 2004 book The Great Influenza: The Epic Story of the Deadliest Plague In History that researchers have found no evidence to support this position.[81] Another theory holds that the 1918 virus mutated extremely rapidly to a less lethal strain. Such evolution of influenza is a common occurrence: there is a tendency for pathogenic viruses to become less lethal with time, as the hosts of more dangerous strains tend to die out.[81] Fatal cases did continue into 1919, however. One notable example was that of ice hockey player Joe Hall, who, while playing for the Montreal Canadiens, fell victim to the flu in April after an outbreak that resulted in the cancellation of the 1919 Stanley Cup Finals.[202] Signs and symptoms 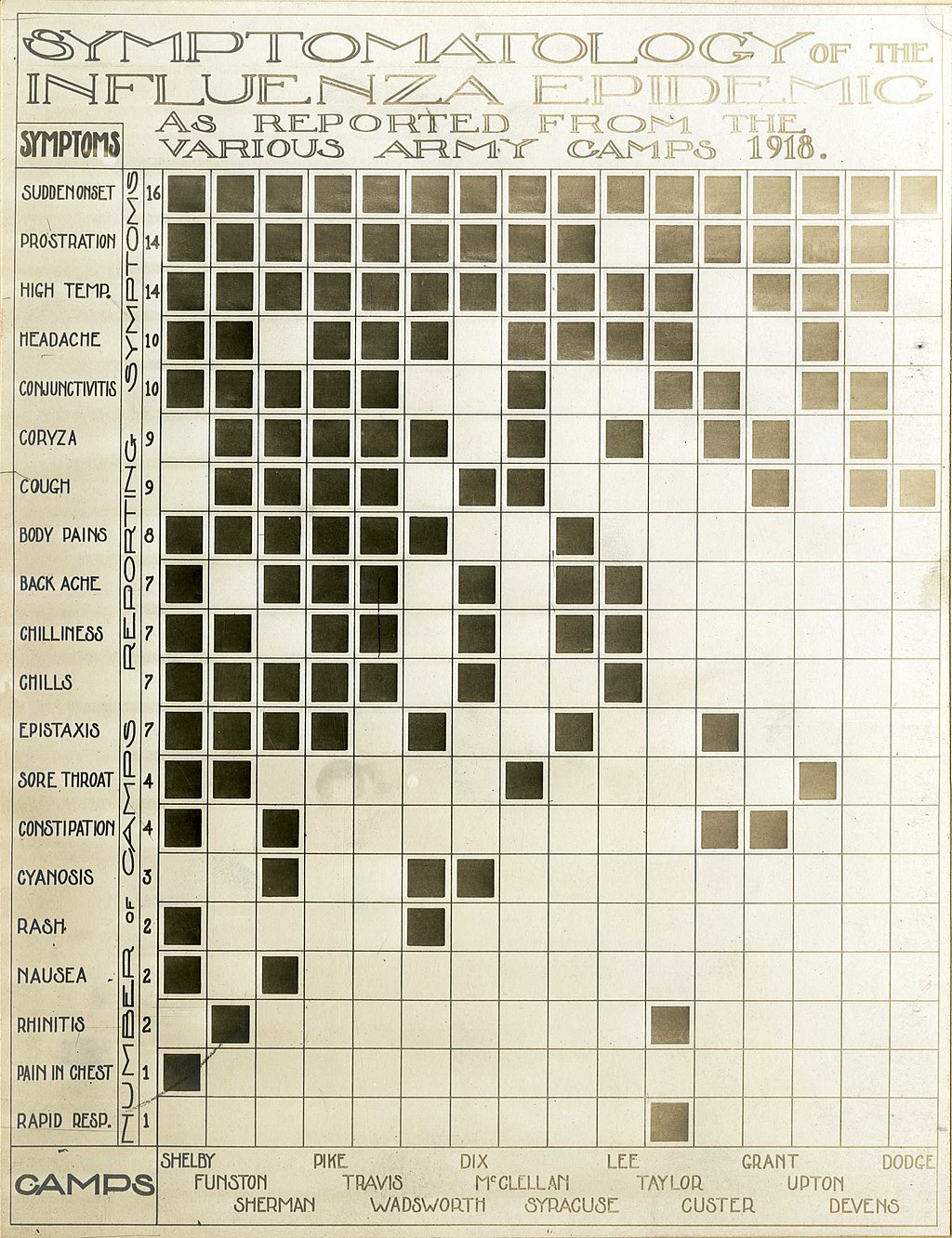 US Army symptomology of the flu The majority of the infected experienced only the typical flu symptoms of sore throat, headache, and fever, especially during the first wave.[203] However, during the second wave, the disease was much more serious, often complicated by bacterial pneumonia, which was often the cause of death.[203] This more serious type would cause heliotrope cyanosis to develop, whereby the skin would first develop two mahogany spots over the cheekbones which would then over a few hours spread to color the entire face blue, followed by black coloration first in the extremities and then further spreading to the limbs and the torso.[203] After this, death would follow within hours or days due to the lungs being filled with fluids.[203] Other signs and symptoms reported included spontaneous mouth and nosebleeds, miscarriages for pregnant women, a peculiar smell, teeth and hair falling out, delirium, dizziness, insomnia, loss of hearing or smell, and impaired vision.[203] One observer wrote, "One of the most striking of the complications was hemorrhage from mucous membranes, especially from the nose, stomach, and intestine. Bleeding from the ears and petechial hemorrhages in the skin also occurred".[204] The majority of deaths were from bacterial pneumonia,[205][206][207] a common secondary infection associated with influenza. This pneumonia was itself caused by common upper respiratory-tract bacteria, which were able to get into the lungs via the damaged bronchial tubes of the victims.[208] The virus also killed people directly by causing massive hemorrhages and edema in the lungs.[207] Modern analysis has shown the virus to be particularly deadly because in animal trials it triggers an overreaction of the body's immune system (sometimes referred to as a cytokine storm).[81] The strong immune reactions of young adults were postulated to have ravaged the body, whereas the weaker immune reactions of children and middle-aged adults resulted in fewer deaths among those groups.[209] Misdiagnosis Because the virus that caused the disease was too small to be seen under a microscope at the time, there were problems with correctly diagnosing it.[210] The bacterium Haemophilus influenzae was instead mistakenly thought to be the cause, as it was big enough to be seen and was present in many, though not all, patients.[210] For this reason, a vaccine that was used against that bacillus did not make an infection rarer but did decrease the death rate.[211] During the deadly second wave there were also fears that it was in fact plague, dengue fever, or cholera.[212] Another common misdiagnosis was typhus, which was common in circumstances of social upheaval, and was therefore also affecting Russia in the aftermath of the October Revolution.[212] In Chile, the view of the country's elite was that the nation was in severe decline, and therefore doctors assumed that the disease was typhus caused by poor hygiene, and not an infectious one, causing a mismanaged response which did not ban mass gatherings.[212] The role of climate conditions  Poster with the slogan: "Coughs and sneezes spread diseases" Studies have shown that the immune system of Spanish flu victims could have been weakened by adverse climate conditions which were particularly unseasonably cold and wet for extended periods of time during the duration of the pandemic. This affected especially WWI troops exposed to incessant rains and lower-than-average temperatures for the duration of the conflict, and especially during the second wave of the pandemic. Ultra-high-resolution climate data combined with highly detailed mortality records analyzed at Harvard University and the Climate Change Institute at the University of Maine identified a severe climate anomaly that impacted Europe from 1914 to 1919, with several environmental indicators directly influencing the severity and spread of the Spanish flu pandemic.[11] Specifically, a significant increase in precipitation affected all of Europe during the second wave of the pandemic, from September to December 1918. Mortality figures follow closely the concurrent increase in precipitation and decrease in temperatures. Several explanations have been proposed for this, including the fact that lower temperatures and increased precipitation provided ideal conditions for virus replication and transmission, while also negatively affecting the immune systems of soldiers and other people exposed to the inclement weather, a factor proven to increase likelihood of infection by both viruses and pneumococcal co-morbid infections documented to have affected a large percentage of pandemic victims (one fifth of them, with a 36% mortality rate).[213][214][215][216][217] A six-year climate anomaly (1914–1919) brought cold, marine air to Europe, drastically changing its weather, as documented by eyewitness accounts and instrumental records, reaching as far as the Gallipoli campaign, in Turkey, where ANZAC troops suffered extremely cold temperatures despite the normally Mediterranean climate of the region. The climate anomaly likely influenced the migration of H1N1 avian vectors which contaminate bodies of water with their droppings, reaching 60% infection rates in autumn.[218][219][220] The climate anomaly has been associated with an anthropogenic increase in atmospheric dust, due to the incessant bombardment; increased nucleation due to dust particles (cloud condensation nuclei) contributed to increased precipitation.[221][222][223] |
疫学と病理学 感染と変異  1918年、ルクセンブルクのホレリッヒ近郊の第29野戦病院における米軍のインフルエンザ患者。米軍がヨーロッパでの戦争に大規模に展開する中、スペイン風邪もまた持ち込まれた。 このウイルスの基本再生産数は2から3の間であった。[193] 第1次世界大戦における密集した状況と大規模な軍隊の移動は、パンデミックを早め、おそらくは感染の拡大と変異の増大を加速させた。また、戦争は人々のウ イルスに対する抵抗力を低下させた可能性もある。兵士たちの免疫システムは栄養失調や戦闘や化学攻撃のストレスによって弱まり、感染しやすくなったという 説もある。[194][195] 世界的なインフルエンザの発生の大きな要因は、旅行の増加であった。近代的な交通システムにより、兵士や水兵、民間人の旅行者が病気を広げやすくなった。 [196] もう一つの要因は、政府による嘘と否定であり、それによって人々は発生に対処する準備ができていなかった。[197] 第2波の深刻さは、第一次世界大戦の状況に起因している。[198] 一般市民の生活においては、自然淘汰は穏やかな株を好む。重篤な症状を呈する者は自宅に留まり、軽症の者は生活を続け、軽症株を優先的に広める。塹壕で は、自然淘汰は逆転した。軽症株の兵士はそのまま留まり、重篤な症状を呈する者は混雑した列車で混雑した野戦病院に送られ、より致死性の高いウイルスを広 めることになった。第2波が始まり、インフルエンザは再び急速に世界中に広がった。そのため、現代のパンデミックにおいては、社会が混乱している地域にウ イルスが到達した際には、保健当局はより致死率の高いウイルス株を捜し求めるようになった。[199] 第1波の感染から回復した人のほとんどが免疫を獲得していたという事実は、同じインフルエンザの株であったに違いないことを示している。これはコペンハー ゲンで最も劇的に示された。コペンハーゲンでは、致死性の低い第1波に感染したことで、死亡率は合計0.29%(第1波では0.02%、第2波では 0.27%)で済んだのである。[200] それ以外の地域では、第2波の致死率ははるかに高かった。最も感染しやすい人々は、塹壕にいる兵士のような人々、つまり若くて健康な成人であった。 [201] 致死率の高い第2波が1918年後半に襲った後、新たな感染者は急激に減少した。例えばフィラデルフィアでは、10月16日までの1週間で4,597人が 死亡したが、11月11日にはインフルエンザはほぼ市内から姿を消した。致死率の急速な低下の理由のひとつとして、ウイルスに感染した後に発症する肺炎の 予防と治療に医師がより効果的になったことが挙げられる。しかし、ジョン・バリーは2004年の著書『The Great Influenza: The Epic Story of the Deadliest Plague In History』の中で、この説を裏付ける証拠は見つかっていないと述べている。[81] 別の説では、1918年のウイルスが致死性の低い株へと急速に変異したというものがある。このようなインフルエンザの進化はよくあることである。病原性ウ イルスは時が経つにつれ致死率が低下する傾向があり、より危険な株の宿主は絶滅する傾向にある。[81] しかし、1919年にも致死例は続いた。注目すべき例としては、モントリオール・カナディアンズでプレーしていたアイスホッケー選手のジョー・ホールが、 1919年のスタンレー・カップ決勝が中止となるほどの流行が発生した後の4月にインフルエンザの犠牲となったことが挙げられる。 兆候と症状  米国陸軍によるインフルエンザの症状学 感染者の大半は、特に最初の流行期には、喉の痛み、頭痛、発熱といった典型的なインフルエンザの症状のみを経験した。[203] しかし、2回目の流行期には、この病気ははるかに深刻になり、細菌性肺炎を併発することが多く、これが死因となることも多かった。[203] このより深刻なタイプでは、ヘリオトロープチアノーゼが発症し、 まず頬骨の上に2つのマホガニー色の斑点が生じ、数時間のうちに顔全体が青く変色し、その後、四肢に黒い色調が現れ、さらに四肢と胴体に広がる。 [203] その後、肺が体液で満たされるため、数時間から数日のうちに死に至る。[203] その他の兆候や 報告されたその他の兆候や症状には、自然に起こる口や鼻からの出血、妊娠中の女性の流産、独特の臭い、歯や髪の抜け落ち、錯乱、めまい、不眠、聴力や嗅覚 の喪失、視力の低下などがあった。ある観察者は、「最も顕著な合併症のひとつは、粘膜、特に鼻、胃、腸からの出血であった。耳からの出血や皮膚の点状出血 も発生した」とある。[204] 死因の大半は細菌性肺炎によるものであった。[205][206][207] これはインフルエンザに付随する一般的な二次感染である。この肺炎は、被害者の損傷した気管支を通って肺に侵入した一般的な上気道細菌によって引き起こさ れた。[208] また、ウイルスは肺に大量出血や浮腫を引き起こすことによっても直接的に人を死に至らしめた。[207] 現代の分析では、ウイルスが特に致死性が高いのは、 動物実験では、このウイルスが免疫システムの過剰反応(サイトカインストームと呼ばれることもある)を引き起こすことが分かっている。[81] 若い成人の強い免疫反応が体を破壊したのに対し、子供や中高年層の弱い免疫反応は、そのグループでの死亡者数の減少につながったと推測されている。 [209] 誤診 当時、この病気を引き起こすウイルスは顕微鏡でも見えないほど小さかったため、正確な診断を下すことが困難であった。目に見えるほど大きく、患者の多くに 存在していたため、インフルエンザ菌が原因であると誤って考えられていた。[210] このため、その細菌に対して使用されていたワクチンは感染を稀にするものではなく、死亡率を低下させるものであった。[211] 致命的な第2波の間には、実際にはペスト、デング熱、コレラではないかという懸念もあった。[212] もう一つの一般的な誤診は発疹チフスであった。これは社会が混乱した状況でよく見られるもので、10月革命後のロシアでも影響を及ぼしていた。[2 12]チリでは、エリート層の間では国民が深刻な衰退状態にあるという見方が一般的であったため、医師たちはこの病気が不衛生が原因のチフスであり、感染 性のものではないと想定し、大規模な集会を禁止しないという不適切な対応をとった。 気候条件の役割  「咳やくしゃみで病気が広がる」というスローガンが書かれたポスター 研究によると、スペイン風邪の犠牲者の免疫システムは、特にパンデミックの期間中に長期間にわたって季節外れの寒さと雨に見舞われた悪条件の気候によって 弱められていた可能性がある。これは、特に第一次世界大戦中の兵士たちに影響を与えた。彼らは、戦時中、特にパンデミックの第2波の間、絶え間ない雨と平 均気温を下回る気温にさらされていた。ハーバード大学とメイン大学気候変動研究所で分析された超高解像度の気候データと詳細な死亡記録を組み合わせたとこ ろ、1914年から1919年にかけてヨーロッパに影響を与えた深刻な気候異常が特定され、いくつかの環境指標がスペイン風邪のパンデミックの深刻さと広 がりに直接影響を与えたことが明らかになった。[11] 具体的には、1918年9月から12月にかけてのパンデミックの第2波の期間に、ヨーロッパ全土で降水量が大幅に増加した。死亡率は、降水量の増加と気温 の低下にほぼ一致して増加した。これにはいくつかの説明が提案されているが、その中には、気温の低下と降水量の増加がウイルスの複製と感染に理想的な条件 をもたらした一方で、悪天候にさらされた兵士やその他の人々の免疫システムに悪影響を与えたという事実も含まれている。この要因は、ウイルスと肺炎球菌の 併発感染の両方による感染の可能性を高めることが証明されており、パンデミックの犠牲者の大半(5分の1、死亡率36%)に影響を与えたことが記録されて いる。[ 213][214][215][216][217] 6年間にわたる気候の異常(1914年~1919年)により、ヨーロッパには冷たく湿った空気が流れ込み、気象が劇的に変化した。これは、目撃者の証言や 機器による記録によって証明されており、トルコのガリポリ戦線にまで及んだ。この地域は通常は地中海性気候であるにもかかわらず、アンザック軍は極度の寒 さに苦しんだ。この気候の異常は、糞によって水場を汚染し、秋には感染率が60%に達したH1N1鳥インフルエンザの媒介生物の移動に影響を与えた可能性 が高い。[218][219][220] この気候の 異常は、絶え間ない砲撃による人為的な大気中の塵の増加と関連している。塵の粒子(雲凝縮核)による核生成の増加が、降水量の増加に寄与した。[221] [222][223] |
| Responses Public health management  Coromandel Hospital Board (New Zealand) advice to influenza sufferers (1918)  In September 1918, the Red Cross recommended two-layer gauze masks to halt the spread of "plague".[224]  1918 Chicago newspaper headlines reflect mitigation strategies such as increased ventilation, arrests for not wearing face masks, sequenced inoculations, limitations on crowd size, selective closing of businesses, curfews, and lockdowns.[225] After October's strict containment measures showed some success, Armistice Day celebrations in November and relaxed attitudes by Thanksgiving caused a resurgence.[225] While systems for alerting public health authorities of infectious spread did exist in 1918, they did not generally include influenza, leading to a delayed response.[226] Nevertheless, actions were taken. Maritime quarantines were declared on islands such as Iceland, Australia, and American Samoa, saving many lives.[226] Social distancing measures were introduced, for example closing schools, theatres, and places of worship, limiting public transportation, and banning mass gatherings.[227] Wearing face masks became common in some places, such as Japan, though there were debates over their efficacy.[227][228] There was also some resistance to their use, as exemplified by the Anti-Mask League of San Francisco. Vaccines were also developed, but as these were based on bacteria and not the actual virus, they could only help with secondary infections.[227] The actual enforcement of various restrictions varied.[229] To a large extent, the New York City health commissioner ordered businesses to open and close on staggered shifts to avoid overcrowding on the subways.[230] A later study found that measures such as banning mass gatherings and requiring the wearing of face masks could cut the death rate up to 50 percent, but this was dependent on their being imposed early in the outbreak and not being lifted prematurely.[231] Medical treatment As there were no antiviral drugs to treat the virus, and no antibiotics to treat the secondary bacterial infections, doctors would rely on a random assortment of medicines with varying degrees of effectiveness, such as aspirin, quinine, arsenics, digitalis, strychnine, epsom salts, castor oil, and iodine.[232] Treatments of traditional medicine, such as bloodletting, ayurveda, and kampo were also applied.[233] Information dissemination Due to World War I, many countries engaged in wartime censorship, and suppressed reporting of the pandemic.[234] For example, the Italian newspaper Corriere della Sera was prohibited from reporting daily death tolls.[235] The newspapers of the time were also generally paternalistic and worried about mass panic.[235] Misinformation also spread along with the disease. In Ireland there was a belief that noxious gases were rising from the mass graves of Flanders Fields and being "blown all over the world by winds".[236] There were also rumors that the Germans were behind it, for example by poisoning the aspirin manufactured by Bayer, or by releasing poison gas from U-boats.[237] |
対応 公衆衛生管理  コロマンデル病院委員会(ニュージーランド)によるインフルエンザ患者への助言(1918年)  1918年9月、赤十字社は「ペスト」の蔓延を食い止めるために2層構造のガーゼマスクを推奨した。[224]  1918年のシカゴの新聞の見出しは、換気量の増加、マスク未着用者の逮捕、順番に予防接種、群衆の人数制限、一部の事業所の閉鎖、夜間外出禁止令、封鎖 といった緩和策を反映している。[225] 10月の厳格な封じ込め策が一定の成果を上げた後、11月の休戦記念日の祝賀と感謝祭による態度の緩和により、再び流行が起こった。[225] 1918年には、感染拡大を公衆衛生当局に警告するシステムは存在していたものの、インフルエンザは一般的に含まれていなかったため、対応が遅れた。 [226] それでも、対策は講じられた。アイスランド、オーストラリア、アメリカ領サモアなどの島々では海上検疫が宣言され、多くの命が救われた。[226] 社会的距離を保つための措置が導入され、例えば、学校、劇場、礼拝所の閉鎖、公共交通機関の利用制限、大規模集会の禁止などが行われた。[2 27] フェイスマスクの着用は、日本など一部の地域では一般的になったが、その有効性については議論があった。[227][228] サンフランシスコのアンチマスクリーグに代表されるように、その使用には抵抗もあった。ワクチンも開発されたが、これらは細菌を基にしており実際のウイル スを基にしたものではなかったため、二次感染の予防にしか役立たなかった。[227] 実際に行われた様々な制限の施行は様々であった。[229] ニューヨーク市の保健局長は、地下鉄の過密を避けるため、企業に対して時差出勤制の導入を命じた。[230] その後の研究では、大規模な集会の禁止やマスクの着用義務などの措置により、死亡率を最大50%削減できる可能性があることが分かったが、これは発生初期にそれらの措置がとられ、早期に解除されなかった場合に限られる。 医療措置 ウイルスを治療する抗ウイルス薬も、二次的な細菌感染を治療する抗生物質もなかったため、医師たちはアスピリン、キニーネ、ヒ素、ジギタリス、ストリキ ニーネ、エプソム塩、ヒマシ油、ヨウ素など、効果の程度が異なるさまざまな薬品を適当に用いた。[232] また、瀉血、アーユルヴェーダ、漢方などの伝統医学による治療も行われた。[233] 情報伝達 第一次世界大戦のため、多くの国が戦時検閲を行い、パンデミックに関する報道を抑制した。[234] 例えば、イタリアの新聞『コリエーレ・デラ・セラ』は、毎日の死者数の報道を禁じられた。[235] 当時の新聞は概して温情主義であり、大衆のパニックを懸念していた。[235] 誤った情報もまた、病気の流行とともに広まった。アイルランドでは、フランダース・フィールドの集団墓地から有毒ガスが立ち上り、「風に乗って世界中に吹 き荒れている」という考えがあった。[236] また、例えばドイツ軍がバイエル社製の頭痛薬アスピリンに毒を混入したり、Uボートから毒ガスを放出したりしているという噂もあった。[237] |
| Mortality See also: List of Spanish flu cases Around the globe 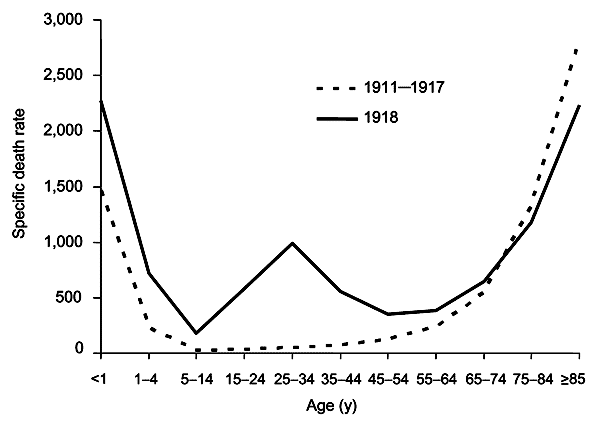 Difference between the flu mortality age-distributions of the 1918 pandemic and normal epidemics – deaths per 100,000 persons in each age group, United States, for the interpandemic years 1911–1917 (dashed line) and the pandemic year 1918 (solid line)[238] 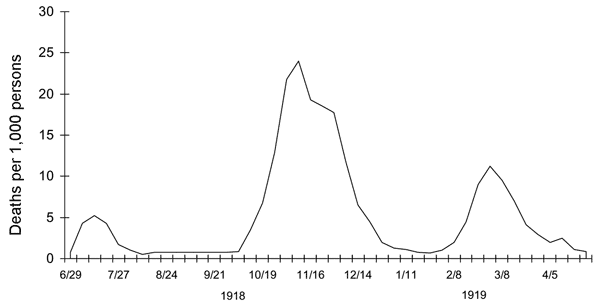 Three pandemic waves: weekly combined flu and pneumonia mortality, United Kingdom, 1918–1919[239] The Spanish flu infected around 500 million people, about one-third of the world's population.[2] Estimates as to how many infected people died vary greatly, but the flu is regardless considered to be one of the deadliest pandemics in history.[240][241] An early estimate from 1927 put global mortality at 21.6 million.[4] An estimate from 1991 states that the virus killed between 25 and 39 million people.[96] A 2005 estimate put the death toll at 50 million (about 3% of the global population), and possibly as high as 100 million (more than 5%).[204][242] However, a 2018 reassessment in the American Journal of Epidemiology estimated the total to be about 17 million,[4] though this has been contested.[243] With a world population of 1.8 to 1.9 billion,[244] these estimates correspond to between 1 and 6 percent of the population. Estimates done in 2021 by John M. Barry have the total death toll alone at well above 100 million.[8] A 2009 study in Influenza and Other Respiratory Viruses based on data from fourteen European countries estimated a total of 2.64 million excess deaths in Europe attributable to the Spanish flu during the major 1918–1919 phase of the pandemic, in line with the three prior studies from 1991, 2002, and 2006 that calculated a European death toll of between 2 million and 2.3 million. This represents a mortality rate of about 1.1% of the European population (c. 250 million in 1918), considerably higher than the mortality rate in the U.S., which the authors hypothesize is likely due to the severe effects of the war in Europe.[121] The excess mortality rate in the U.K. has been estimated at 0.28%–0.4%, far below this European average.[4] Some 12–17 million people died in India, about 5% of the population.[245] The death toll in India's British-ruled districts was 13.88 million.[246] Another estimate gives at least 12 million dead.[247] The decade between 1911 and 1921 was the only census period in which India's population fell, mostly due to devastation of the Spanish flu pandemic.[248][249] While India is generally described as the country most severely affected by the Spanish flu, at least one study argues that other factors may partially account for the very high excess mortality rates observed in 1918, citing unusually high 1917 mortality and wide regional variation (ranging from 0.47% to 6.66%).[4] A 2006 study in The Lancet also noted that Indian provinces had excess mortality rates ranging from 2.1% to 7.8%, stating: "Commentators at the time attributed this huge variation to differences in nutritional status and diurnal fluctuations in temperature."[250] In Finland, 20,000 died out of 210,000 infected.[251] In Sweden, 34,000 died.[252] In Japan, the flu killed nearly 500,000 people over two waves between 1918 and 1920, with nearly 300,000 excess deaths between October 1918 and May 1919 and 182,000 between December 1919 and May 1920.[146] In the Dutch East Indies (now Indonesia), 1.5 million were assumed to have died among 30 million inhabitants.[253] In Tahiti, 13% of the population died during one month. Similarly, in Western Samoa 22% of the population of 38,000 died within two months.[254] In Istanbul, capital of the Ottoman Empire, 6,403[255] to 10,000[102] died, giving the city a mortality rate of at least 0.56%.[255] In New Zealand, the flu killed an estimated 6,400 Pākehā (or "New Zealanders primarily of European descent") and 2,500 indigenous Māori in six weeks, with Māori dying at eight times the rate of Pākehā.[256][257] In Australia, the flu killed around 12,000[258] to 20,000 people.[259] The country's death rate, 2.7 per 1,000 people, was one of the lowest recorded compared with other countries at the time; however, as much as 40 percent of the population were infected, and a mortality rate of 50 percent was recorded by some Aboriginal communities.[260][259] New South Wales and Victoria saw the greatest relative mortality, with 3.19 and 2.40 deaths per 1,000 people respectively, while Western Australia, Queensland, Southern Australia, and Tasmania experienced rates of 1.70, 1.14, 1.13, and 1.09 per 1,000 respectively. In Queensland, at least one-third of deaths recorded were in the Aboriginal population.[125] In the U.S., about 28% of the population of 105 million became infected, and 500,000 to 850,000 died (0.48 to 0.81 percent of the population).[261][262][263] Native American tribes were particularly hard hit. In the Four Corners area, there were 3,293 registered deaths among Native Americans.[264] Entire Inuit and Alaskan Native village communities died in Alaska.[265] In Canada, 50,000 died.[266] In Brazil, 300,000 died, including president Rodrigues Alves.[267] In the UK, as many as 250,000 died; in France, more than 400,000.[268] In Ghana, the influenza epidemic killed at least 100,000 people.[269] Tafari Makonnen (the future Haile Selassie, Emperor of Ethiopia) was one of the first Ethiopians who contracted influenza but survived.[270][271] Many of his subjects did not; estimates for fatalities in the capital city, Addis Ababa, range from 5,000 to 10,000, or higher.[272] The death toll in Russia has been estimated at 450,000, though the epidemiologists who suggested this number called it a "shot in the dark".[96] If it is correct, Russia lost roughly 0.4% of its population, meaning it suffered the lowest influenza-related mortality in Europe. Another study considers this number unlikely, given that the country was in the grip of a civil war, and the infrastructure of daily life had broken down; the study suggests that Russia's death toll was closer to 2%, or 2.7 million people.[273] Devastated communities 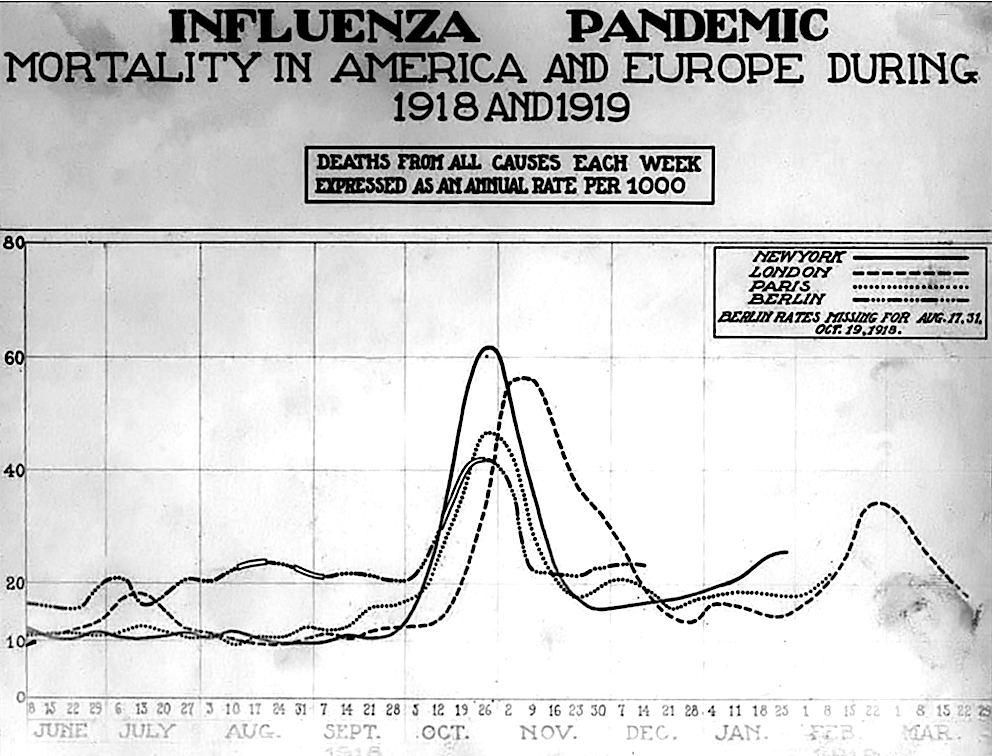 Deaths from all causes for New York, London, Paris, and Berlin with peaks in October and November 1918 Even in areas where mortality was low, so many adults were incapacitated that much of everyday life was hampered. Some communities closed all stores or required customers to leave orders outside. There were reports that healthcare workers could not tend the sick nor the gravediggers bury the dead because they too were ill. Mass graves were dug by steam shovel and bodies buried without coffins in many places.[274] Bristol Bay, a region of Alaska populated by indigenous people, suffered a death rate of 40 percent of the total population, with some villages entirely disappearing.[275] Nenana, Alaska, managed to avoid the extent of the pandemic between 1918 and 1919, but the flu at last reached the town in spring 1920. Reports suggested that during the first two weeks of May, the majority of the town's population became infected; 10% of the population were estimated to have died, most of whom were Alaska Natives.[276] Several Pacific island territories were hit particularly hard. The pandemic reached them from New Zealand, which was too slow to implement measures to prevent ships, such as Talune, carrying the flu from leaving its ports. From New Zealand, the flu reached Tonga (killing 8% of the population), Nauru (16%), and Fiji (5%, 9,000 people).[277] Worst affected was Western Samoa, formerly German Samoa, which had been occupied by New Zealand in 1914. 90% of the population was infected; 30% of adult men, 22% of adult women, and 10% of children died. By contrast, Governor John Martin Poyer prevented the flu from reaching neighboring American Samoa by imposing a blockade.[277] The disease spread fastest through the higher social classes among the indigenous peoples, because of the custom of gathering oral tradition from chiefs on their deathbeds; many community elders were infected through this process.[278] In Iran, the mortality was very high: according to an estimate, between 902,400 and 2,431,000, or 8% to 22% of the total population died.[279] The country was going through the Persian famine of 1917–1919 concurrently. In Ireland, during the worst 12 months, the Spanish flu accounted for one-third of all deaths.[280][281] In South Africa it is estimated that about 300,000 people amounting to 6% of the population died within six weeks. Government actions in the early stages of the virus' arrival in the country in September 1918 are believed to have unintentionally accelerated its spread throughout the country.[282] Almost a quarter of the working population of Kimberley, consisting of workers in the diamond mines, died.[283] In British Somaliland, one official estimated that 7% of the native population died.[284] This huge death toll resulted from an extremely high infection rate of up to 50% and the extreme severity of the symptoms.[96] Other areas In the Pacific, American Samoa[285] and the French colony of New Caledonia[286] succeeded in preventing even a single death from influenza through effective quarantines. However, the outbreak was delayed into 1926 for American Samoa and 1921 for New Caledonia as the quarantine period ended.[287] On American Samoa, at least 25% of the island residents were clinically attacked and 0.1% died, and on New Caledonia, there was widespread illness and 0.1% population died.[287] Australia also managed to avoid the first two waves with a quarantine.[226] Iceland protected a third of its population from exposure by blocking the main road of the island.[226] By the end of the pandemic, the isolated island of Marajó, in Brazil's Amazon River Delta had not reported an outbreak.[288] Saint Helena also reported no deaths.[289]  Japanese women in Tokyo during the Spanish flu pandemic, 1919 Estimates for the death toll in China have varied widely,[290][96] a range which reflects the lack of centralized collection of health data at the time due to the Warlord period. China may have experienced a relatively mild flu season in 1918 compared to other areas of the world.[190][174][291] However, some reports from its interior suggest that mortality rates from influenza were perhaps higher in at least a few locations in China in 1918.[273] At the very least, there is little evidence that China as a whole was seriously affected by the flu compared to other countries in the world.[292] The first estimate of the Chinese death toll was made in 1991 by Patterson and Pyle, which estimated a toll of between 5 and 9 million. However, this 1991 study was criticized by later studies due to flawed methodology, and newer studies have published estimates of a far lower mortality rate in China.[188][293] For instance, Iijima in 1998 estimates the death toll in China to be between 1 and 1.28 million based on data available from Chinese port cities.[294] The lower estimates of the Chinese death toll are based on the low mortality rates that were found in Chinese port cities (for example, Hong Kong) and on the assumption that poor communications prevented the flu from penetrating the interior of China.[290] However, some contemporary newspaper and post office reports, as well as reports from missionary doctors, suggest that the flu did penetrate the Chinese interior and that influenza was severe in at least some locations in the countryside of China.[273] Although medical records from China's interior are lacking, extensive medical data were recorded in Chinese port cities, such as then British-controlled Hong Kong, Canton, Peking, Harbin and Shanghai. These data were collected by the Chinese Maritime Customs Service, which was largely staffed by non-Chinese foreigners, such as the British, French, and other European colonial officials in China.[295] As a whole, data from China's port cities show low mortality rates compared to other cities in Asia.[295] For example, the British authorities at Hong Kong and Canton reported a mortality rate from influenza at a rate of 0.25% and 0.32%, much lower than the reported mortality rate of other cities in Asia, such as Calcutta or Bombay, where influenza was much more devastating.[295] Similarly, in the city of Shanghai – which had a population of over 2 million in 1918 – there were only 266 recorded deaths from influenza among the Chinese population in 1918.[295] If extrapolated from the extensive data recorded from Chinese cities, the suggested mortality rate from influenza in China as a whole in 1918 was likely lower than 1% – much lower than the world average (which was around 3–5%).[295] In contrast, Japan and Taiwan had reported a mortality rate from influenza around 0.45% and 0.69% respectively, higher than the mortality rate collected from data in Chinese port cities, such as Hong Kong (0.25%), Canton (0.32%), and Shanghai.[295] However, it is noted that the influenza mortality rate in Hong Kong and Canton are under-recorded, because only the deaths that occurred in colony hospitals were counted.[295] Similarly, in Shanghai, these statistics are limited to that area of the city under the control of the health section of the Shanghai International Settlement, and the actual death toll in Shanghai was much higher.[295] The medical records from China's interior indicate that, compared to cities, rural communities have substantially higher mortality rate.[296] A published influenza survey in Houlu County, Hebei Province, found that the case fatality rate was 9.77% and 0.79% of county population died from influenza in October and November 1918.[297] Patterns of fatality 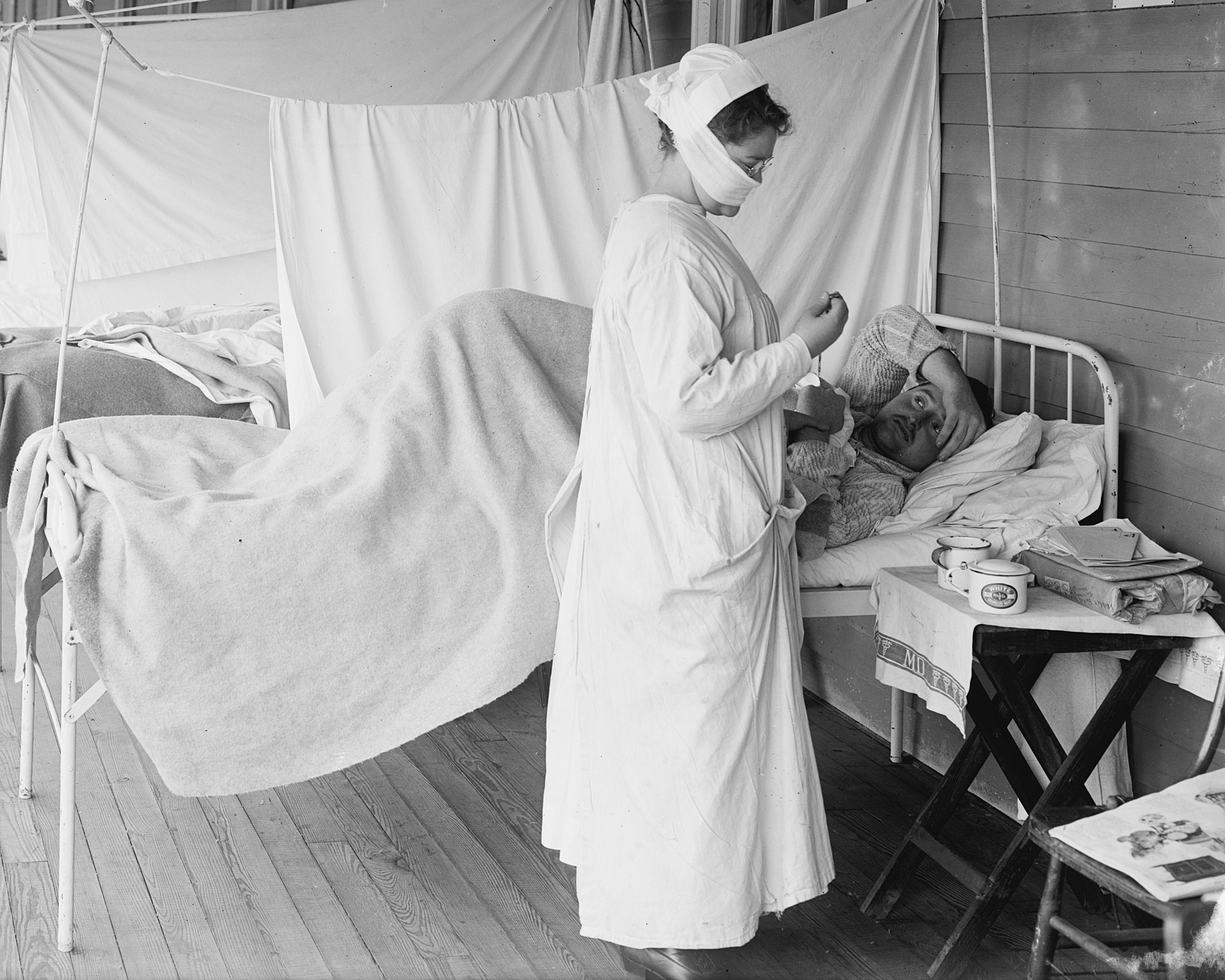 A nurse wears a cloth face mask while treating a flu patient in Washington, DC, c. 1919 The pandemic mostly killed young adults. In 1918–1919, 99% of pandemic influenza deaths in the U.S. occurred in people under 65, and nearly half of deaths were in young adults 20 to 40 years old. In 1920, the mortality rate among people under 65 had decreased sixfold to half the mortality rate of people over 65, but 92% of deaths still occurred in people under 65.[298] This is unusual since influenza is typically most deadly to weak individuals, such as infants under age two, adults over age 70, and the immunocompromised. In 1918, older adults may have had partial protection caused by exposure to the 1889–1890 flu pandemic, known as the "Russian flu".[299] According to historian John M. Barry, the most vulnerable of all – "those most likely, of the most likely", to die – were pregnant women. He reported that in thirteen studies of hospitalized women in the pandemic, the death rate ranged from 23% to 71%.[300] Of the pregnant women who survived childbirth, over one-quarter (26%) lost the child.[301] Another oddity was that the outbreak was widespread in the summer and autumn (in the Northern Hemisphere); influenza is usually worse in winter.[302] There were also geographic patterns to the disease's fatality. Some parts of Asia had 30 times higher death rates than some parts of Europe, and generally, Africa and Asia had higher rates, while Europe and North America had lower ones.[303] There was also great variation within continents, with three times higher mortality in Hungary and Spain compared to Denmark, two to three times higher chance of death in Sub-Saharan Africa compared to North Africa, and possibly up to ten times higher rates between the extremes of Asia.[303] Cities were affected worse than rural areas.[303] There were also differences between cities, which might have reflected exposure to the milder first wave giving immunity, as well as the introduction of social distancing measures.[304] Another major pattern was the differences between social classes. In Oslo, death rates were inversely correlated with apartment size, as the poorer people living in smaller apartments died at a higher rate.[305] Social status was also reflected in the higher mortality among immigrant communities, with Italian Americans, a recently arrived group at the time, were nearly twice as likely to die compared to the average Americans.[303] These disparities reflected worse diets, crowded living conditions, and problems accessing healthcare.[303] Paradoxically, however, African Americans were relatively spared by the pandemic.[303] More men than women were killed by the flu, as they were more likely to go out and be exposed, while women would tend to stay at home.[304] For the same reason men also were more likely to have pre-existing tuberculosis, which severely worsened the chances of recovery.[304] However, in India the opposite was true, potentially because Indian women were neglected with poorer nutrition, and were expected to care for the sick.[304] A study conducted by He et al. (2011) used a mechanistic modeling approach to study the three waves of the 1918 influenza pandemic. They examined the factors that underlie variability in temporal patterns and their correlation to patterns of mortality and morbidity. Their analysis suggests that temporal variations in transmission rate provide the best explanation, and the variation in transmission required to generate these three waves is within biologically plausible values.[306] Another study by He et al. (2013) used a simple epidemic model incorporating three factors to infer the cause of the three waves of the 1918 influenza pandemic. These factors were school opening and closing, temperature changes throughout the outbreak, and human behavioral changes in response to the outbreak. Their modeling results showed that all three factors are important, but human behavioral responses showed the most significant effects.[307] |
死亡率 参照:スペイン風邪の症例一覧 世界全体  1918年のパンデミックと通常の流行におけるインフルエンザによる死亡率の年齢分布の違い - 1911年から1917年の間(破線)と1918年のパンデミックの年(実線)における、各年齢層における10万人当たりの死亡者数(米国)[238]  3つのパンデミック波:イギリスにおけるインフルエンザと肺炎による死亡率の週ごとの合計、1918年~1919年[239] スペイン風邪は、世界の人口の約3分の1にあたる約5億人を感染させた。[2] 感染者のうち何人が死亡したかについては推定値に大きな幅があるが、このインフルエンザは歴史上最も致命的なパンデミックのひとつであると考えられてい る。[240][241] 1927年の初期の推定では、世界的な死亡率は21 。1991年の推定では、ウイルスによる死者は2500万人から3900万人とされている。[96] 2005年の推定では、死者数は5000万人(世界人口の約3%)で、最大で1億人(5%以上)に達する可能性があるとしている。[204][ ][242] しかし、2018年の『アメリカ疫学ジャーナル』誌での再評価では、その総数は約1700万人と推定されているが[4]、これには異論もある[243]。 世界人口が18億から19億人であることを踏まえると[244]、これらの推定値は人口の1パーセントから6パーセントに相当する。 ジョン・M・バリーが2021年に行った推定では、死亡者総数は1億人を超えるとされている。 14のヨーロッパ諸国のデータに基づく2009年の『インフルエンザとその他の呼吸器ウイルス』誌の研究では、1918年から1919年のパンデミックの 主要な時期に、スペイン風邪が原因でヨーロッパで264万人の超過死亡があったと推定されている。 1918年から1920年にかけてのパンデミックのピーク時に、ヨーロッパで200万から230万人の死者が出たという1991年、2002年、2006 年の3つの先行研究と一致する。これはヨーロッパ人口(1918年当時約2億5000万人)の約1.1%にあたる死亡率であり、著者はこの死亡率がヨー ロッパでの戦争の深刻な影響によるものである可能性が高いと仮説を立てている。[121] イギリスでの超過死亡率は0.28%から0.4%と推定されており、このヨーロッパ平均をはるかに下回っている。[4] インドでは約1,200万人から1,700万人が死亡し、これは人口の約5%にあたる。[245] 英国統治下のインドでの死者数は1,388万人であった。[246] 別の推計では少なくとも1,200万人が死亡したとしている。[247] 1911年から1921年までの10年間は 1921年の間は、インドの人口が減少した唯一の国勢調査期間であり、その主な原因はスペイン風邪の大流行による被害であった。[248][249] インドは一般的に、スペイン風邪による被害が最も深刻だった国として説明されているが、少なくとも1つの研究では、1918年に観察された非常に高い超過 死亡率は、他の要因が部分的に原因である可能性があると主張している 1917年の死亡率が異常に高く、地域差が大きかった(0.47%から6.66%の範囲)ことを挙げている。[4] 2006年の『ランセット』誌に掲載された研究でも、インドの州ごとの死亡率の差異は2.1%から7.8%の範囲であったことが指摘され、「当時のコメン テーターたちは、この大きな差異を栄養状態の差異と日中の気温の変動に帰していた」と述べている。[250] フィンランドでは、感染者21万人のうち2万人が死亡した。[251] スウェーデンでは3万4千人が死亡した。[252] 日本では、1918年から1920年の2回の流行で、50万人近くが死亡した。1918年10月から1919年5月までの間では30万人近く、1919年12月から1920年5月までの間では18万2000人が、インフルエンザによる超過死亡者であった。 オランダ領東インド(現在のインドネシア)では、3,000万人の人口のうち150万人が死亡したと推定されている。[253] タヒチでは、人口の13%が1か月間で死亡した。同様に、西サモアでは3万8,000人の人口のうち22%が2か月間で死亡した。[254] オスマン帝国の首都イスタンブールでは、6,403人から10,000人が死亡し、死亡率は少なくとも0.56%であった。 ニュージーランドでは、6週間で推定6,400人のパケハ(または「主にヨーロッパ系ニュージーランド人」)と2,500人の先住民マオリが死亡し、マオリの死亡率はパケハの8倍であった。 オーストラリアでは、インフルエンザにより1万2000人から2万人が死亡したとされる。[258][259] 人口1000人当たりの死亡率は2.7人と、当時としては記録上最も低い数値であったが、人口の40パーセントが感染し、死亡率50パーセントという数字 がいくつかのアボリジニのコミュニティで記録された。。ニュー・サウス・ウェールズ州とビクトリア州では、1,000人あたり3.19人と2.40人の死 亡者がでており、最も高い死亡率を示した。一方、西オーストラリア州、クイーンズランド州、南オーストラリア州、タスマニア州では、それぞれ1,000人 あたり1.70人、1.14人、1.13人、1.09人の死亡率であった。クイーンズランド州では、記録された死亡者の少なくとも3分の1がアボリジニで あった。[125] 米国では、人口1億500万人のうち約28%が感染し、50万から85万人が死亡した(人口の0.48から0.81%)。[261][262][263] アメリカ先住民部族は特に大きな打撃を受けた。フォーコーナーズ地域では、ネイティブアメリカンによる登録死亡者数は3,293人に上った。[264] アラスカではイヌイットとアラスカ先住民の村社会全体が壊滅した。[265] カナダでは50,000人が死亡した。[266] ブラジルでは、ロドリゲス・アルヴェス大統領を含む300,000人が死亡した。[267] イギリスでは25万人、フランスでは40万人以上が死亡した。 ガーナでは、インフルエンザの流行により少なくとも10万人が死亡した。タファリ・マコンネン(後のエチオピア皇帝ハイレ・セラシエ)は、インフルエンザ に感染したが生き延びた最初のエチオピア人の一人であった 。[270][271] 彼の臣民の多くは生き残れなかった。首都アディスアベバでの推定死者数は5,000人から10,000人、あるいはそれ以上である。[272] ロシアにおける死者数は45万人と推定されているが、この数字を提示した疫学者は「当てずっぽう」と述べている。[96] この数字が正しいとすると、ロシアでは人口のおよそ0.4%が失われたことになり、ヨーロッパ諸国の中で最もインフルエンザ関連の死亡率が低かったことに なる。別の研究では、ロシア国内では内戦が続いており、日常生活のインフラも崩壊していたことを踏まえ、この数字はありそうもないと見ている。この研究で は、ロシアの死者数は2%に近い、つまり270万人であったと示唆している。 荒廃した地域社会  1918年10月と11月にピークを迎えたニューヨーク、ロンドン、パリ、ベルリンの全死因による死亡者数 死亡率が低かった地域でも、多くの成人が衰弱したため、日常生活のほとんどが妨げられた。一部の地域では、すべての店舗が閉店したり、顧客が注文を店先に 置いていくことを余儀なくされた。医療従事者も病人の世話をすることができず、墓堀人も病気のために死者を埋葬することができなかったという報告もあっ た。多くの場所で、蒸気ショベルで集団墓地が掘られ、棺に入れられずに遺体が埋葬された。 先住民が住むアラスカのブリストル湾地域では、人口の40パーセントが死亡し、いくつかの村は完全に消滅した。 アラスカのネナナは、1918年から1919年のパンデミックの規模をなんとか免れたが、ついに1920年春にインフルエンザがこの町にも到達した。5月 の最初の2週間の間に、町の人口の大半が感染し、人口の10%が死亡したと推定され、その大半はアラスカ先住民であったと報告されている。 太平洋諸島地域の一部は特に大きな打撃を受けた。ニュージーランドからパンデミックが到来したが、同国はタルーネ号のようなインフルエンザを運ぶ船を阻止 するための措置を講じるのが遅すぎた。ニュージーランドから、トンガ(人口の8%が死亡)、ナウル(16%)、フィジー(5%、9,000人)にインフル エンザが到達した。[277] 最も大きな被害を受けたのは、1914年にニュージーランドが占領した旧ドイツ領サモアの西サモアであった。人口の90%が感染し、成人男性の30%、成 人女性の22%、そして子供の10%が死亡した。これに対し、ジョン・マーティン・ポイヤー総督は封鎖を実施することで、インフルエンザが隣接するアメリ カ領サモアに到達するのを防いだ。[277] この病気は、先住民の中でも社会的地位の高い階級の間で最も急速に広がった。これは、長老が死の床で口頭伝承を収集するという習慣があったためであり、多 くのコミュニティの長老がこの過程で感染した。[278] イランでは死亡率が非常に高く、推定では総人口の8%から22%にあたる902,400人から2,431,000人が死亡したとされる。[279] 同国では1917年から1919年にかけてペルシア飢饉が起こっていた。 アイルランドでは、最悪の12か月間において、スペイン風邪による死亡者数は全死亡者数の3分の1を占めた。 南アフリカでは、人口の6%にあたる約30万人が6週間以内に死亡したと推定されている。1918年9月にウイルスが国内に到達した初期段階における政府 の対応が、意図せずして国内での感染拡大を加速させたと考えられている。[282] ダイヤモンド鉱山の労働者で構成されるキンバリー市の労働人口のほぼ4分の1が死亡した 。[283] イギリス領ソマリランドでは、ある役人が推定で人口の7%が死亡したと述べている。[284] この膨大な死者数は、感染率が最大で50%に達したことと、症状が極めて深刻だったことによるものである。[96] その他の地域 太平洋地域では、アメリカ領サモア[285]とフランス領ニューカレドニア[286]が効果的な隔離により、インフルエンザによる死者を1人も出さずに防 ぐことに成功した。しかし、アメリカ領サモアでは1926年まで、ニューカレドニアでは1921年まで流行が遅れた。これは隔離期間が終了したためであ る。アメリカ領サモアでは、少なくとも島民の25%が臨床的に感染し、0.1%が死亡した。また、ニューカレドニアでは、広範囲にわたって感染が拡大し、 人口の0.1%が死亡した。オーストラリアもまた、最初の2つの波を検疫によって回避することができた。[226] アイスランドは、島の主要道路を封鎖することで、人口の3分の1を感染から守った。[226] 大流行の終息までに、ブラジルのアマゾン川デルタにある孤立したマラジョー島では、感染の発生は報告されなかった。[288] セントヘレナ島でも死亡者は報告されていない。[289]  1919年のスペイン風邪流行時の東京の日本人女性 中国における死亡者数の推定値は大きく異なっているが[290][96]、これは軍閥時代に健康データの集中収集が行われなかったことを反映している。中 国では、1918年のインフルエンザの流行は、世界の他の地域と比較して比較的軽度であった可能性がある[190][174][291]。しかし、中国内 陸部からのいくつかの報告では、1918年のインフルエンザによる死亡率は、 1918年の中国では、少なくともいくつかの地域ではインフルエンザによる死亡率がより高かった可能性があることを示唆する報告もある。[273] 少なくとも、中国全体が世界中の他の国々と比較してインフルエンザに深刻な影響を受けたという証拠はほとんどない。[292] 中国における最初の死者数推定値は、1991年にパターソンとパイルによって行われたもので、500万人から900万人の死者数と推定された。しかし、こ の1991年の研究は、その後の研究によってその方法論の欠陥が指摘され、批判された。より新しい研究では、中国の死亡率ははるかに低いと推定されてい る。[188][293] 例えば、飯島は1998年に、中国の港湾都市で入手可能なデータに基づいて、中国の死者数を100万から128万人と推定している。[294] 中国の死者数の低い推定値は、 死亡率が低かった中国の港湾都市(例えば香港)のデータと、通信手段が不十分だったために中国内陸部にはインフルエンザが侵入しなかったという仮定に基づ いて算出されている。[290] しかし、当時の新聞や郵便局の報告書、宣教師医師の報告書などによると、インフルエンザは中国内陸部にも侵入しており、少なくとも中国農村部の一部の地域 ではインフルエンザが深刻な被害をもたらしていたことが示唆されている。[273] 中国内陸部の医療記録は残っていないが、当時イギリスが支配していた香港、広州、北京、ハルビン、上海などの中国の港湾都市では、広範囲にわたる医療デー タが記録されていた。これらのデータは、主に中国人以外の外国人、例えばイギリス人、フランス人、その他のヨーロッパの植民地官僚によって占められていた 中国海関によって収集された。[295] 全体として、中国の港湾都市のデータは、アジアの他の都市と比較して死亡率が低いことを示している。[295] 例えば、香港と広州のイギリス当局は インフルエンザによる死亡率はそれぞれ0.25%、0.32%と報告されており、これはインフルエンザが猛威を振るったカルカッタやボンベイなど、アジア の他の都市で報告された死亡率よりもはるかに低い数字であった。[295] 同様に、1918年の人口が200万人を超えていた上海では、 1918年の中国人のインフルエンザによる死亡者数は266人に留まった。[295] 中国の都市で記録された膨大なデータから推定すると、1918年の中国全体でのインフルエンザによる死亡率は1%以下であった可能性が高い。これは世界平 均(3~5%程度)よりもはるかに低い数値である。3~5%)であった。[295] これに対し、日本と台湾では、それぞれ0.45%、0.69%というインフルエンザによる死亡率が報告されており、香港(0.25%)、広東 (0.32%)、上海(0.25%)といった中国の港湾都市のデータから収集された死亡率よりも高かった。[295] しかし、香港と広州のインフルエンザ死亡率は過小評価されている。植民地の病院で死亡した患者のみが数えられたためである。[295] 同様に、上海では、これらの統計は上海国際租界の衛生部門が管理する市内の地域に限られており、実際の死者数ははるかに多かった。[295] 中国内陸部の医療記録によると、都市部と比較して農村部の死亡率は大幅に高いことが示されている。[296] 中国内陸部の医療記録によると、都市部と比較して農村部の死亡率が大幅に高いことが示されている。[296] 河北省の霍鹿県で実施されたインフルエンザ調査では、1918年10月と11月の死亡率が9.77%で、同県の人口の0.79%がインフルエンザで死亡し たことが分かった。[297] 致死率のパターン  ワシントンD.C.で、インフルエンザ患者の治療中に布製のマスクを着用する看護師(1919年頃) パンデミックでは主に若い成人が死亡した。1918年から1919年にかけて、米国におけるパンデミック・インフルエンザによる死亡者の99%は65歳未 満の人々であり、死亡者のほぼ半数は20歳から40歳までの若い成人であった。1920年には、65歳未満の死亡率は6倍から65歳以上の死亡率の半分に 減少したが、それでも死亡者の92%は65歳未満であった。[298] これは異常なことで、インフルエンザは通常、2歳未満の乳児、70歳以上の成人、免疫不全者など、体力のない人々に最も致命的な影響を与える。1918年 当時、高齢者には、1889年から1890年にかけて発生した「ロシア風邪」として知られるインフルエンザの大流行にさらされた経験から、ある程度の免疫 があった可能性がある。[299] 歴史家のジョン・M・バリーによると、最も死亡の危険性が高かったのは、最も可能性の高い人々、つまり、妊娠中の女性であった。彼は、パンデミック時に入 院した女性を対象とした13件の研究において、死亡率は23%から71%の範囲であったと報告している。[300] 出産後に生き残った妊婦のうち、4分の1以上(26%)が子供を失った。[301] もう一つの奇妙な点は、この流行が夏と秋(北半球)に広がったことである。インフルエンザは通常、冬に悪化する。[302] 死亡率には地理的なパターンも見られた。アジアの一部地域ではヨーロッパの一部地域よりも死亡率が30倍高く、一般的にアフリカとアジアの死亡率は高く、 ヨーロッパと北米では低かった。[303] 大陸内でも大きなばらつきがあり、ハンガリーとスペインではデンマークと比較して死亡率が3倍高く、サハラ以南のアフリカでは北アフリカと比較して2~3 倍高い死亡率となり、アジアの極端な地域間では最大で10倍高い死亡率となった可能性もある。 サハラ以南のアフリカでは北アフリカと比較して2~3倍、アジアの極端な地域間では最大10倍の死亡率となっている可能性もある。[303] 都市部は農村部よりも深刻な影響を受けた。[303] 都市間でも違いが見られ、これは、より穏やかな第1波にさらされたことで免疫が得られたことや、社会的距離の確保策が導入されたことなどが反映されている 可能性がある。[304] もう一つの大きなパターンは、社会階級間の違いであった。オスロでは、死亡率はアパートの広さと逆相関関係にあり、狭いアパートに住む貧困層の人々の死亡 率が高かった。[305] 社会的地位は、移民コミュニティにおける死亡率の高さにも反映されており、当時、最近到着したグループであったイタリア系アメリカ人は 、平均的なアメリカ人と比較して2倍近く死亡する可能性が高かった。[303] これらの格差は、不健康な食生活、過密な生活環境、医療へのアクセスの問題を反映していた。[303] しかし、逆説的ではあるが、アフリカ系アメリカ人はこのパンデミックから比較的免れた。[303] 外出して感染する可能性が高い男性の方が、女性よりも多く死亡した。一方、女性は家にいる傾向があった。[304] 同じ理由で、男性は結核を患っている可能性も高く、回復の可能性を著しく低下させた。[304] しかし、インドでは逆のことが起こった。これは、インドの女性は栄養状態が悪く、病人を看病することが期待されていたためである可能性がある。[304] He ら(2011年)による研究では、1918年のインフルエンザ・パンデミックの3つの波を研究するために、メカニズム・モデリング・アプローチが用いられ た。彼らは、時間的パターンの変動の根底にある要因と、死亡率および罹患率のパターンとの相関関係を調査した。彼らの分析は、感染率の時間的変動が最も良 い説明を提供し、この3つの波を発生させるのに必要な感染率の変動は生物学的に妥当な値の範囲内であることを示唆している。[306] また、Heらによる別の研究(2013年)では、1918年のインフルエンザパンデミックの3つの波の原因を推測するために、3つの要因を組み込んだ単純 な流行モデルを使用した。これらの要因は、学校の開校と休校、流行期間中の気温の変化、そして流行に対する人間の行動の変化であった。彼らのモデリングの 結果、3つの要因すべてが重要であることが示されたが、人間の行動反応が最も大きな影響を示した。[307] |
| Effects World War I Academic Andrew Price-Smith has made the argument that the virus helped tip the balance of power in the latter days of the war towards the Allied cause. He provides data that the viral waves hit the Central Powers before the Allied powers and that both morbidity and mortality in Germany and Austria were considerably higher than in Britain and France.[183] A 2006 Lancet study corroborates higher excess mortality rates in Germany (0.76%) and Austria (1.61%) compared to Britain (0.34%) and France (0.75%).[250] Kenneth Kahn at Oxford University Computing Services writes that "Many researchers have suggested that the conditions of the war significantly aided the spread of the disease. And others have argued that the course of the war (and subsequent peace treaty) was influenced by the pandemic." Kahn has developed a model that can be used on home computers to test these theories.[308] Economic  Provincial Board of Health poster from Alberta, Canada Many businesses in the entertainment and service industries suffered losses in revenue, while the healthcare industry reported profit gains.[309] Historian Nancy Bristow has argued that the pandemic, when combined with the increasing number of women attending college, contributed to the success of women in the field of nursing. This was due in part to the failure of medical doctors, who were predominantly men, to contain and prevent the illness. Nursing staff, who were mainly women, celebrated the success of their patient care and did not associate the spread of the disease with their work.[310] A 2020 study found that U.S. cities that implemented early and extensive non-medical measures (quarantine, etc.) suffered no additional adverse economic effects due to implementing those measures.[311][312] However, the validity of this study has been questioned because of the coincidence of WWI and other problems with data reliability.[313] Long-term effects A 2006 study in the Journal of Political Economy found that "cohorts in utero during the pandemic displayed reduced educational attainment, increased rates of physical disability, lower income, lower socioeconomic status, and higher transfer payments received compared with other birth cohorts."[314] A 2018 study found that the pandemic reduced educational attainment in populations.[315] The flu has also been linked to the outbreak of encephalitis lethargica in the 1920s.[316] Survivors faced an elevated mortality risk. Some survivors did not fully recover from physiological conditions resulting from infection.[317] Legacy  Mass burial site of flu victims from 1918 in Auckland, New Zealand Despite the high morbidity and mortality rates that resulted from the epidemic, the Spanish flu began to fade from public awareness over the decades until the arrival of news about bird flu and other pandemics in the 1990s and 2000s.[318][319] This has led some historians to label the Spanish flu a "forgotten pandemic".[175] However, this label has been challenged by the historian Guy Beiner, who has charted a complex history of social and cultural forgetting, demonstrating how the pandemic was overshadowed by the commemoration of the First World War and mostly neglected in mainstream historiography, yet was remembered in private and local traditions across the globe.[319] There are various theories of why the Spanish flu was "forgotten". The rapid pace of the pandemic, which killed most of its victims in the United States within less than nine months, resulted in limited media coverage. The general population was familiar with patterns of pandemic disease in the late 19th and early 20th centuries: typhoid, yellow fever, diphtheria, and cholera all occurred near the same time. These outbreaks probably lessened the significance of the influenza pandemic for the public.[320] In some areas, the flu was not reported on, the only mention being that of advertisements for medicines claiming to cure it.[321] Additionally, the outbreak coincided with the deaths and media focus on the First World War.[322] Another explanation involves the age group affected by the disease. The majority of fatalities, from both the war and the epidemic, were among young adults. The high number of war-related deaths of young adults may have overshadowed the deaths caused by flu.[298] When people read the obituaries, they saw the war or postwar deaths and the deaths from the influenza side by side. Particularly in Europe, where the war's toll was high, the flu may not have had a tremendous psychological impact or may have seemed an extension of the war's tragedies.[298] The duration of the pandemic and the war could have also played a role. The war, however, had initially been expected to end quickly but lasted for four years by the time the pandemic struck. In literature and other media  US comic published in 1922. Despite the toll of the pandemic, it was never a large theme in American literature.[323] Alfred Crosby suspects that it may be due to the fact that it occurred after World War I, which was the most important event in that generation's lives.[324] Katherine Anne Porter's 1939 novella Pale Horse, Pale Rider is one of the most well-known fictional accounts of the pandemic.[323] The 2006 novel The Last Town on Earth focuses on a town which attempts to limit the spread of the flu by preventing people from entering or leaving.[325] The Pull of the Stars is a 2020 novel by Emma Donoghue set in Dublin during the Spanish flu. Its final draft was submitted in March 2020, and publishers fast-tracked publication because of the then ongoing COVID-19 pandemic.[326] Comparison with other pandemics The Spanish flu killed a much lower percentage of the world's population than the Black Death, which lasted for many more years.[327] The recent COVID-19 pandemic is estimated to have killed 17.5 - 31.4 million.[328] 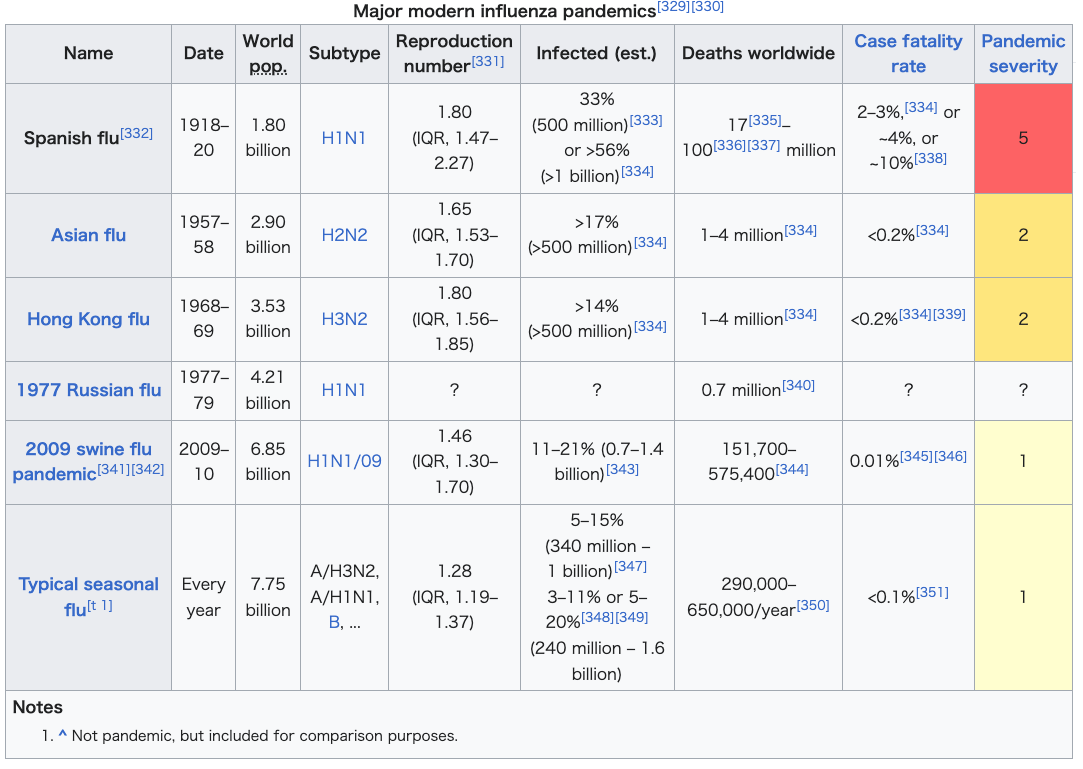 |
影響 第一次世界大戦 学術界のアンドリュー・プライス・スミスは、ウイルスが戦争末期の戦況を連合国の勝利に傾けるのに役立ったという主張を行っている。彼は、ウイルスの波が 連合国よりも先に中央同盟国を襲ったこと、また、ドイツとオーストリアにおける罹患率と死亡率が、イギリスとフランスよりもかなり高かったことを示すデー タを提示している。[183] 2006年の『ランセット』誌の研究では、イギリス(0.34%)とフランス(0.75%)に比べ、ドイツ(0.76%)とオーストリア(1.61%)で 高い超過死亡率が確認された。[250] オックスフォード大学コンピューティングサービス部のケネス・カーンは、「多くの研究者が、戦争の状況が病気の蔓延を著しく助長したと指摘している。ま た、戦争の経過(およびその後の講和条約)がパンデミックの影響を受けたという意見もある」と書いている。カーンは、これらの理論を検証するために家庭用 コンピューターで使用できるモデルを開発した。 経済  カナダ、アルバータ州の経済省保健局のポスター 娯楽産業やサービス産業の多くの企業が収益の減少に見舞われた一方で、医療業界は利益の増加を報告した。[309] 歴史家のナンシー・ブリストウは、パンデミックと大学進学する女性の増加が相まって、看護の分野における女性の成功に貢献したと主張している。これは、男 性が大半を占めていた医師たちが、この病気の封じ込めと予防に失敗したことも一因である。看護スタッフは主に女性であったが、患者ケアの成功を祝う一方 で、この病気の蔓延を自分たちの仕事と関連付けることはなかった。 2020年の研究では、早期に広範囲にわたる非医療措置(隔離など)を実施した米国の都市では、それらの措置を実施したことによる追加的な悪影響は経済に は及ばなかったことが分かった。[311][312] しかし、第一次世界大戦やその他の問題がデータ信頼性と重なっていたため、この研究の妥当性は疑問視されている。[313] 長期的な影響 2006年の『Journal of Political Economy』誌に掲載された研究では、「パンデミック時に胎内にいた世代は、他の出生コホートと比較して、教育達成度の低下、身体障害率の上昇、低所 得、低社会経済的地位、受給額の多い移転支出が認められた」ことが分かった。 314] 2018年の研究では、パンデミックにより人口の教育達成度が低下したことが分かった。[315] また、インフルエンザは1920年代の嗜眠性脳炎の発生とも関連している。[316] 生存者は死亡率の上昇というリスクに直面した。感染による生理学的状態から完全に回復しなかった生存者もいた。[317] 遺産  ニュージーランドのオークランドにある1918年のインフルエンザ犠牲者の集団埋葬地 スペイン風邪は、その高い罹患率と死亡率にもかかわらず、1990年代と2000年代に鳥インフルエンザやその他のパンデミックに関するニュースが報道さ れるまで、数十年にわたって人々の意識から忘れられつつあった。[318][319] そのため、一部の歴史家はスペイン風邪を「忘れられたパンデミック」と呼んでいる 。しかし、このレッテルは歴史家のガイ・ベイナーによって否定されている。ベイナーは、社会と文化における複雑な忘却の歴史を明らかにし、このパンデミッ クが第一次世界大戦の記念行事によって影が薄くなり、主流の歴史学ではほとんど顧みられなかったが、世界中の個人や地域の伝統では記憶されていたことを示 している。 スペイン風邪が「忘れ去られた」理由については、さまざまな説がある。このパンデミックは急速に進行し、犠牲者の大半は9か月足らずの間に米国で死亡した ため、メディアの報道も限定的なものにとどまった。19世紀後半から20世紀初頭にかけて、腸チフス、黄熱病、ジフテリア、コレラなどのパンデミックがほ ぼ同時期に発生していたため、一般の人々はこうした流行病のパターンに慣れていた。こうした流行病の発生により、恐らく一般の人々にとってインフルエン ザ・パンデミックの重大性は薄れてしまったのである。[320] 地域によっては、インフルエンザの発生は報道されず、インフルエンザを治療すると謳った薬の広告が掲載されただけだった。[321] さらに、この流行は第一次世界大戦による死者の発生とメディアの注目と重なっていた。[322] 別の説明としては、この病気に罹患した年齢層が関係している。 戦争と流行の両方による死者の大半は、若い成人であった。 若い成人の戦争関連の死者の数が多かったため、インフルエンザによる死者が影が薄くなってしまった可能性がある。[298] 人々が死亡記事を読んだとき、彼らは戦争や戦後の死とインフルエンザによる死が並んで掲載されているのを目にした。特に戦争による犠牲者が多かったヨー ロッパでは、インフルエンザは心理的にそれほど大きな衝撃を与えなかったか、あるいは戦争の悲劇の延長のように思われたのかもしれない。[298] パンデミックと戦争が同時に起こったことも、心理的な影響を弱めた可能性がある。しかし、当初はすぐに終結すると思われていた戦争は、パンデミックが猛威 を振るう頃には4年間にわたって続いていた。 文学やその他のメディアでは  1922年に出版された米国の漫画。 パンデミックによる犠牲にもかかわらず、アメリカ文学では決して大きなテーマとはならなかった。[323] アルフレッド・クロスビーは、その原因はパンデミックが第一次世界大戦後に発生したためであり、その世代の生活において最も重要な出来事であったためでは ないかと推測している。[324] キャサリン・アン・ポーターの1939年の小説『Pale Horse, Pale Rider』は、 パンデミックを題材としたフィクション作品として最もよく知られているもののひとつである。[323] 2006年の小説『The Last Town on Earth』は、人々の出入りを制限することでインフルエンザの蔓延を食い止めようとする町に焦点を当てている。[325] 『The Pull of the Stars』は、スペイン風邪の流行中のダブリンを舞台にした、エマ・ドナヒューによる2020年の小説である。2020年3月に最終稿が提出され、当時 進行中であった新型コロナウイルス感染症のパンデミックのため、出版社は出版を早めた。 他のパンデミックとの比較 スペイン風邪は、何年も続いた黒死病よりも、世界の人口に占める死亡者の割合がはるかに低かった。 最近の新型コロナウイルス感染症によるパンデミックでは、1750万人から3140万人が死亡したと推定されている。  |
| Research Main article: Spanish flu research 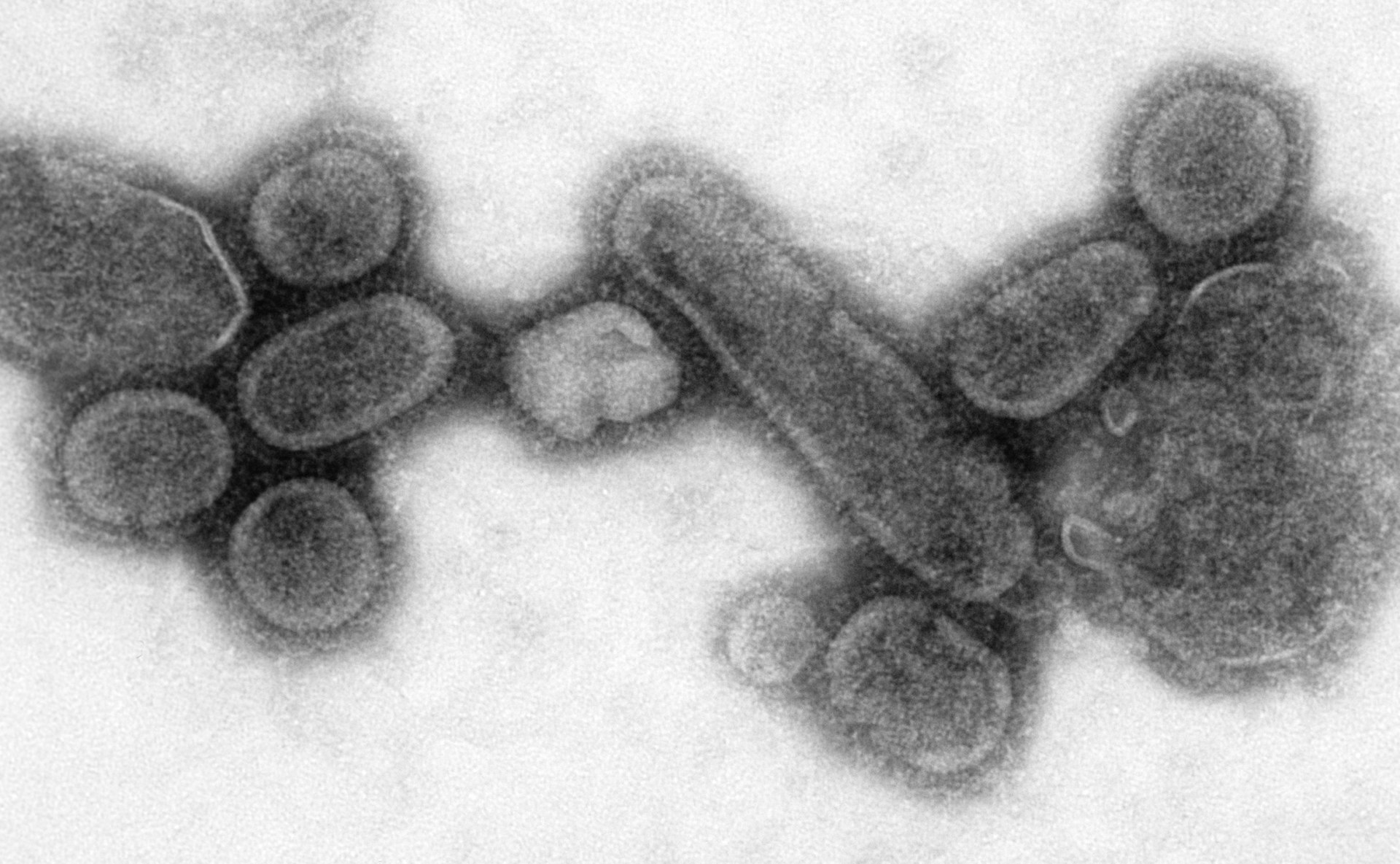 An electron micrograph showing recreated 1918 influenza virions The origin of the Spanish flu pandemic, and the relationship between the near-simultaneous outbreaks in humans and swine, have been controversial. One hypothesis is that the virus strain originated at Fort Riley, Kansas, in viruses in poultry and swine which the fort bred for food; the soldiers were then sent from Fort Riley around the world, where they spread the disease.[352] Similarities between a reconstruction of the virus and avian viruses, combined with the human pandemic preceding the first reports of influenza in swine, led researchers to conclude the influenza virus jumped directly from birds to humans, and swine caught the disease from humans.[353][354] Others have disagreed,[355] and more recent research has suggested the strain may have originated in a nonhuman, mammalian species.[356] An estimated date for its appearance in mammalian hosts has been put at the period 1882–1913.[357] This ancestor virus diverged about 1913–1915 into two clades (or biological groups each descended from a common ancestor), which gave rise to the classical swine and human H1N1 influenza lineages. The last common ancestor of human strains dates between February 1917 and April 1918. Because pigs are more readily infected with avian influenza viruses than are humans, they were suggested as the original recipients of the virus, passing the virus to humans sometime between 1913 and 1918.  Dr Terrence Tumpey examines a reconstructed version of the Spanish flu virus at the CDC An effort to recreate the Spanish flu strain (a strain of influenza A subtype H1N1) was a collaboration among the Armed Forces Institute of Pathology, the USDA ARS Southeast Poultry Research Laboratory, and Mount Sinai School of Medicine in New York City. The effort resulted in the announcement (on 5 October 2005) that the group had successfully determined the virus' genetic sequence, using historic tissue samples recovered by pathologist Johan Hultin from an Inuit female flu victim buried in the Alaskan permafrost and samples preserved from American soldiers[358] Roscoe Vaughan and James Downs.[359][360][354] This enabled researchers at the Centers for Disease Control and Prevention (CDC) and the Mount Sinai School of Medicine, led by Dr Terrence Tumpey, to synthesize RNA segments from the H1N1 virus and ultimately reconstruct infective virus particles.[361] These were subsequently used to experimentally infect mice, ferrets, and macaques giving valuable insights into influenza virus biology and pathogenesis, providing important information about how to prevent and control future pandemics.[362] On 18 January 2007, Kobasa et al. (2007) reported that monkeys (Macaca fascicularis) infected with the recreated flu strain exhibited classic symptoms of the 1918 pandemic, and died from an overreaction of the immune system.[363] This may explain why the Spanish flu had its surprising effect on younger, healthier people, as a person with a stronger immune system would potentially have a stronger overreaction.[364] In December 2008, research by Yoshihiro Kawaoka of the University of Wisconsin linked the presence of three specific genes (termed PA, PB1, and PB2) and a nucleoprotein derived from Spanish flu samples to the ability of the 1918 flu virus to invade the lungs and cause pneumonia. These genes were inserted into a modern H1N1 strain and triggered similar symptoms in animal testing.[365] In 2008 an investigation used the virus sequence to obtain the Hemagglutinin (HA) antigen and observe the adaptive immunity in 32 survivors of the 1918 flu pandemic, all of them presented seroreactivity and 7 of 8 further tested presented memory B cells able to produce antibodies that bound to the HA antigen highlighting the ability of the immunological memory many decades after.[366][354] In June 2010, a team at the Mount Sinai School of Medicine reported the 2009 flu pandemic vaccine provided some cross-protection against the Spanish flu pandemic strain.[367] One of the few things known for certain about influenza in 1918 and for some years after was that it was, except in the laboratory, exclusively a disease of human beings.[368] In 2013, the AIR Worldwide Research and Modeling Group "characterized the historic 1918 pandemic and estimated the effects of a similar pandemic occurring today using the AIR Pandemic Flu Model". In the model, "a modern-day 'Spanish flu' event would result in additional life insurance losses of between US$15.3–27.8 billion in the United States alone", with 188,000–337,000 deaths in the United States.[369] In 2018, Michael Worobey, an evolutionary biology professor at the University of Arizona who is examining the history of the 1918 pandemic, revealed that he obtained tissue slides created by William Rolland, a physician who reported on a respiratory illness likely to be the virus while a pathologist in the British military during World War One.[370] Rolland had authored an article in the Lancet during 1917 about a respiratory illness outbreak beginning in 1916 in Étaples, France.[371][372] Worobey traced recent references to that article to family members who had retained slides that Rolland had prepared during that time. Worobey extracted tissue from the slides to potentially reveal more about the origin of the pathogen.[28] Sex differences in mortality The high mortality rate of the influenza pandemic is one aspect that sets the pandemic apart from other disease outbreaks. Another factor is the higher mortality rate of men compared with women. Men with an underlying condition were at significantly more risk. Tuberculosis was one of the deadliest diseases in the 1900s, and killed more men than women. But with the spread of influenza disease, the cases of tuberculosis cases in men decreased. Many scholars have noted that tuberculosis increased the mortality rate of influenza in males, decreasing their life expectancy. During the 1900s tuberculosis was more common in males than females, but studies show that when influenza spread the tuberculosis mortality rate among females changed. The death rate of tuberculosis in females increased significantly and would continue to decline until post-pandemic.[373] Death rates were particularly high in those aged 20–35. The only comparable disease to this was the Black Death, or bubonic plague, in the 1300s. As other studies have shown, tuberculosis and influenza had comorbidities and one affected the other. The ages of males dying of the flu show that tuberculosis was a factor, and as males primarily had this disease at the time of the pandemic, they had a higher mortality rate. Life expectancy dropped in males during the pandemic but then increased two years after the pandemic.[374] Island of Newfoundland One major cause of the spread of influenza was social behavior. Men had more social variation and were mobile more than women due to their work. Even though there was a higher mortality rate in males, each region showed different results, due to such factors as nutritional deficiency. In Newfoundland, the pandemic spread was highly variable. Influenza did not discriminate who was infected, indeed it attacked the socioeconomic status of people. Although social variability allowed the disease to move quickly geographically, it tended to spread faster and affect men more than women due to labor and social contact. Newfoundland's leading cause of death before the pandemic was tuberculosis and this is known to be a severe underlying condition for people and increases the |mortality rate when infected by the influenza disease. There was diverse labor in Newfoundland, men and women had various occupations that involved day-to-day interaction. But, fishing had a major role in the economy and so males were more mobile than females and had more contact with other parts of the world. The spread of the pandemic is known to have begun in the spring of 1918, but Newfoundland did not see the deadly wave until June or July, which aligns with the high demand for employment in the fishery. The majority of men were working along the coast during the summer and it was typical for entire families to move to Newfoundland and work. Studies show a much higher mortality rate in males compared with females. But, during the first, second, and third waves of the pandemic, the mortality shifted. During the first wave, men had a higher mortality rate, but the mortality rate of females increased and was higher during the second and third waves. The female population was larger in certain regions of Newfoundland and therefore had a bigger impact on the death rate.[375] Influenza pandemic among Canadian soldiers Records indicate the most deaths during the first wave of the pandemic were among young men in their 20s, which reflects the age of enlistment in the war. The mobility of young men during 1918 was linked to the spread of influenza and the biggest wave of the epidemic. In late 1917 and throughout 1918, thousands of male troops gathered at the Halifax port before heading to Europe. Any soldier that was ill and could not depart was added to the population of Halifax, which increased the case rate of influenza among men during the war. To determine the cause of the death during the pandemic, war scientists used the Commonwealth War Graves Commission (CWGC), which reported under 2 million men and women died during the wars, with a record of those who died from 1917 to 1918. The movement of soldiers during this time and the transportation from United States between Canada likely had a significant effect on the spread of the pandemic.[376] |
研究 詳細はスペイン風邪の研究を参照  1918年のインフルエンザウイルス粒子を再現した電子顕微鏡写真 スペイン風邪のパンデミックの起源と、ほぼ同時期にヒトとブタの間で発生したこととの関連性については、議論の的となってきた。一つの仮説は、カンザス州 フォート・ライリーの砦で、食料として飼育していた家禽やブタのウイルスからウイルス株が発生したというもので、その後、フォート・ライリーから兵士たち が世界中に派遣され、そこで病気が広まったというものである。ウイルスの再構成と鳥類のウイルスとの類似性、および豚におけるインフルエンザの最初の報告 に先立つヒトの世界的大流行を併せて考えると、研究者はインフルエンザウイルスが鳥類からヒトへと直接感染し、豚はヒトから感染したと結論づけた。 [353][354] これに反対する意見もあるが[355]、より最近の研究では、この株は非ヒト哺乳類種に由来する可能性が示唆されている。 3年であると推定されている。[357] この祖先ウイルスは1913年から1915年頃に2つのクレード(共通の祖先から分岐した生物学的グループ)に分岐し、これが古典的なブタおよびヒトの H1N1インフルエンザ系統を生み出した。ヒトの株の最後の共通祖先は、1917年2月から1918年4月の間とされている。豚はヒトよりも鳥インフルエ ンザウイルスに感染しやすいため、豚がウイルスの最初の宿主となり、1913年から1918年の間にヒトにウイルスが感染した可能性が示唆された。  CDCでスペイン風邪ウイルスの復元版を調べるテレンス・タンピー博士 スペイン風邪(インフルエンザA亜型H1N1)の株を再現する試みは、軍病理学研究所、米国農務省農業研究局南東家禽研究施設、ニューヨーク市にあるマウ ント・サイナイ医科大学の共同作業であった。この努力の結果、2005年10月5日に、グループがウイルスの遺伝子配列を決定することに成功したことが発 表された。これは、病理学者ヨハン・ハルティンがアラスカの永久凍土に埋葬されていたインディアンの女性インフルエンザ犠牲者から回収した歴史的な組織サ ンプルと、アメリカ兵のロスコー・ヴォーンとジェームズ・ダウンズから保存されていたサンプルを使用したものである。 これにより、テレンス・タンプリー博士率いる疾病対策予防センター(CDC)とシナイ山医学校の研究者が、H1N1ウイルスからRNA断片を合成し、最終 的に感染性ウイルス粒子を再構成することが可能となった。[361] これらはその後、マウス、フェレット、マカク属に実験的に感染させるために使用され、インフルエンザウイルスの生物学と病原性に関する貴重な洞察が得ら れ、将来のパンデミックを予防し制御する方法に関する重要な情報が提供された。[362] 2007年1月18日、Kobasaら(2007年)は、再現されたインフルエンザ株に感染したサル(マカク属)が1918年のパンデミックの典型的な症 状を示し、 免疫システムの過剰反応により死亡した。[363] スペイン風邪が健康な若年層にも驚くほどの影響を与えた理由を説明できるかもしれない。免疫システムが強力な人ほど、より強い過剰反応を起こす可能性があ るからだ。[364] 2008年12月、ウィスコンシン大学の河岡義裕による研究では、1918年のインフルエンザウイルスが肺に侵入し肺炎を引き起こす能力と、スペイン風邪 のサンプルから得られた3つの特定の遺伝子(PA、PB1、PB2と呼ばれる)と核タンパク質との関連性が指摘された。これらの遺伝子は現代のH1N1株 に挿入され、動物実験で同様の症状を引き起こした。 2008年の調査では、ウイルスの遺伝子配列からヘマグルチニン(HA)抗原を入手し、1918年のインフルエンザ大流行の生存者32人の適応免疫を観察 した。その結果、全員が血清反応を示し、さらに検査した8人中7人がHA抗原に結合する抗体を産生できるメモリーB細胞を示し、免疫記憶の能力が数十年後 に発揮されることが明らかになった。[366][354] 2010年6月、マウント・サイナイ医科大学の研究チームは、2009年の新型インフルエンザワクチンがスペイン風邪のパンデミック株に対してある程度の交差防御効果があることを報告した。 1918年のインフルエンザについて、またその数年後について確実に分かっていることのひとつは、実験室を除いては、インフルエンザはもっぱらヒトの病気であったということである。 2013年、AIRワールドワイド・リサーチ・モデリンググループは「1918年の歴史的なパンデミックの特徴を明らかにし、AIRパンデミック・インフ ルエンザ・モデルを使用して、今日同様のパンデミックが発生した場合の影響を推定した」。このモデルでは、「現代の『スペイン風邪』の流行は、米国だけで 153億ドルから278億ドルの生命保険の損失を追加で生じさせる」と推定されており、米国では18万8000人から33万7000人が死亡するとされて いる。 2018年、1918年のパンデミックの歴史を研究しているアリゾナ大学の進化生物学教授マイケル・ウォロベイは、第一次世界大戦中にイギリス軍の病理学 者として、ウイルスによる可能性が高い呼吸器疾患について報告した医師、ウィリアム・ロランが作成した組織スライドを入手したことを明らかにした 。ロールは1917年に医学誌『ランセット』に、1916年にフランス・エタプルで発生した呼吸器疾患の流行に関する記事を執筆していた。[371] [372] ウォロベイは、その記事に関する最近の参考文献を辿り、ロールが当時作成したスライドを保管していた家族の元を訪れた。ウォロベイはスライドから組織を採 取し、病原体の起源についてさらに多くの情報を引き出す可能性がある。[28] 死亡率における性差 インフルエンザ・パンデミックにおける死亡率の高さは、パンデミックを他の感染症の流行と区別する特徴のひとつである。もうひとつの要因は、女性よりも男 性の方が死亡率が高いことである。基礎疾患を持つ男性は、リスクが著しく高かった。結核は1900年代に最も致命的な病気のひとつであり、男性の死亡率が 女性のそれを上回っていた。しかし、インフルエンザの流行に伴い、男性の結核患者数は減少した。多くの学者が、結核は男性のインフルエンザによる死亡率を 高め、平均余命を縮めることを指摘している。1900年代には結核は男性に多く見られたが、研究によると、インフルエンザが蔓延すると女性の結核死亡率に 変化が見られた。女性の結核死亡率は著しく上昇し、パンデミック後まで低下しなかった。 死亡率は特に20歳から35歳で高かった。これと比較できる病気は、1300年代に流行した黒死病、すなわちペストだけである。他の研究でも示されている ように、結核とインフルエンザは併発し、一方が他方に影響を及ぼしていた。インフルエンザで死亡した男性の年齢を見ると、結核が要因であったことが示され ており、パンデミック発生当時は主に男性がこの病気にかかっていたため、死亡率が高かった。パンデミックの間、男性の平均余命は減少したが、パンデミック 後2年で増加した。[374] ニューファンドランド島 インフルエンザの拡大の主な原因の一つは社会行動であった。男性は女性よりも仕事のために社会的な変動が多く、移動性も高かった。男性の死亡率が高かった とはいえ、栄養不足などの要因により、各地域で異なる結果が示された。ニューファンドランドでは、パンデミックの拡大は地域によって大きな差があった。イ ンフルエンザは感染者を差別することはなく、人々の社会経済的地位を襲った。社会的な変動性により、この病気は地理的に急速に広がったが、労働や社会的な 接触により、女性よりも男性の方がより急速に感染し、影響を受けやすかった。パンデミック以前のニューファンドランドの主な死因は結核であり、これは人々 にとって深刻な基礎疾患であることが知られており、インフルエンザに感染すると死亡率が上昇する。ニューファンドランドではさまざまな労働があり、男女と もにさまざまな職業に就いており、日常的に交流があった。しかし、経済においては漁業が大きな役割を果たしていたため、男性の方が女性よりも移動性が高 く、世界の他の地域との接触も多かった。パンデミックの拡大は1918年の春に始まったことが知られているが、ニューファンドランドでは6月か7月まで致 命的な感染の波が到来しなかった。これは、漁業における雇用需要の高まりと一致している。夏の間、大半の男性は沿岸で働いており、家族全員がニューファン ドランドに移住して働くことは一般的であった。研究によると、男性の死亡率は女性よりもはるかに高い。しかし、パンデミックの第1波、第2波、第3波の間 では、死亡率に変化が見られた。第1波では男性の死亡率が高かったが、第2波と第3波では女性の死亡率が上昇し、高くなった。ニューファンドランドの特定 の地域では女性の人口が多かったため、死亡率への影響が大きかった。[375] カナダ軍兵士の間でのインフルエンザの流行 記録によると、パンデミックの第1波による死者の大半は20代の若い男性であった。これは、戦争における入隊年齢を反映している。1918年の若い男性の 流動性は、インフルエンザの拡大と、流行の最大波と関連していた。1917年後半から1918年にかけて、数千人の男性兵士がヨーロッパに向かう前にハリ ファックス港に集結した。病気で出発できない兵士は、ハリファックスの人口に加えられ、戦争中の男性のインフルエンザ感染率が上昇した。パンデミックによ る死因を特定するために、戦争科学者たちは連邦戦争墓地委員会(CWGC)を利用した。同委員会は、戦争中に死亡した男女の数は200万人を下回ると報告 し、1917年から1918年にかけて死亡した人数を記録した。この時期の兵士の移動と、カナダと米国間の輸送が、パンデミックの拡大に大きな影響を与え た可能性が高い。[376] |
| 1918 flu pandemic in India – Known in India as "Bombay Fever" 2009 swine flu pandemic – 2009–2010 pandemic of swine influenza caused by H1N1 influenza virus Anti-Mask League of San Francisco – 1919 San Francisco organization COVID-19 pandemic – Pandemic caused by SARS-CoV-2 Pandemic – Widespread, often global, epidemic of severe infectious disease List of epidemics List of Spanish flu cases |
1918年にインドで大流行したインフルエンザ - インドでは 「ボンベイ・フィーバー 」として知られている。 2009年豚インフルエンザの大流行 - H1N1インフルエンザウイルスによる2009年から2010年の豚インフルエンザの大流行。 サンフランシスコ反マスク連盟 - 1919年サンフランシスコの組織 COVID-19パンデミック - SARS-CoV-2によるパンデミック。 パンデミック - 広範囲に、しばしば世界的に、深刻な感染症が流行する。 伝染病のリスト スペイン風邪の症例リスト |
| https://en.wikipedia.org/wiki/Spanish_flu |
|
リ ンク
文 献
そ の他の情報
Copyleft,
CC, Mitzub'ixi Quq Chi'j, 1996-2099