Fear and Pleasure
Fear and Pleasure

★「生物学的な恐怖反応は非常に複雑であ り、扁桃体から前頭葉まで、さまざまな脳領域に影響を与える神経伝達物質とホルモンが関係している。……われわれの体は、恐ろしいものに対して、闘うか逃 げるための準備をするよう進化してきた。具体的には、瞳孔を広げてものがよく見えるようにしたり、気管支を広げて酸素を多く取り込めるようにしたり、血液 やブドウ糖を重要な器官や骨格筋に送り込んだりする。」
☆「アドレナリン、ドーパミン、コルチ ゾールは、人間が脅威を感じたときに放出する3つの重要な物質……。危険を察知すると、アドレナリンの放出によってわれわれの「闘争・逃走反応」が引き起 こされる。これによって心拍数、血圧、呼吸数などが高まる。……ストレスホルモンであるコルチゾールは、体のさまざまな機能を調節するために常時放出され ている。しかし、何らかの状況や経験を乗り越えようと緊張したときには、その量が一気に増える。……コルチゾールは、まずアドレナリンなどの「闘争・逃 走」ホルモンが一気に放出された後も警戒が維持されるのを助ける。また、緊急事態の最中に、肝臓からエネルギーとなるブドウ糖(グルコース)が放出される のを促す。(コルチゾールのレベルが慢性的に高い状態は身体によいわけではない)。……アドレナリンとコルチゾールは、どちらもストレスと関係がある。ス トレスは、胸痛、頭痛や震え、疲労、筋肉の緊張といった身体的な症状のほか、いらつき、パニック発作、悲しみといった感情的な症状(を起こす)。ドーパミ ンは、より全般的に良い気分をもたらす神経伝達物質だ。これは喜びや、報酬の期待や経験などに関連しており(これが、恐怖の後の高揚感と関係しているかも しれない)」
「恐怖の対象が目の前から消えて初めて ドーパミンが放出されるわけではない。報酬への期待感があれば放出される……。薬物依存症の患者は、目当ての薬がまだ手元になくとも、それを追い求めてい る最中に、ドーパミンによって高揚感を経験する(のではないかと考えられている)」https://x.gd/0HYyT.
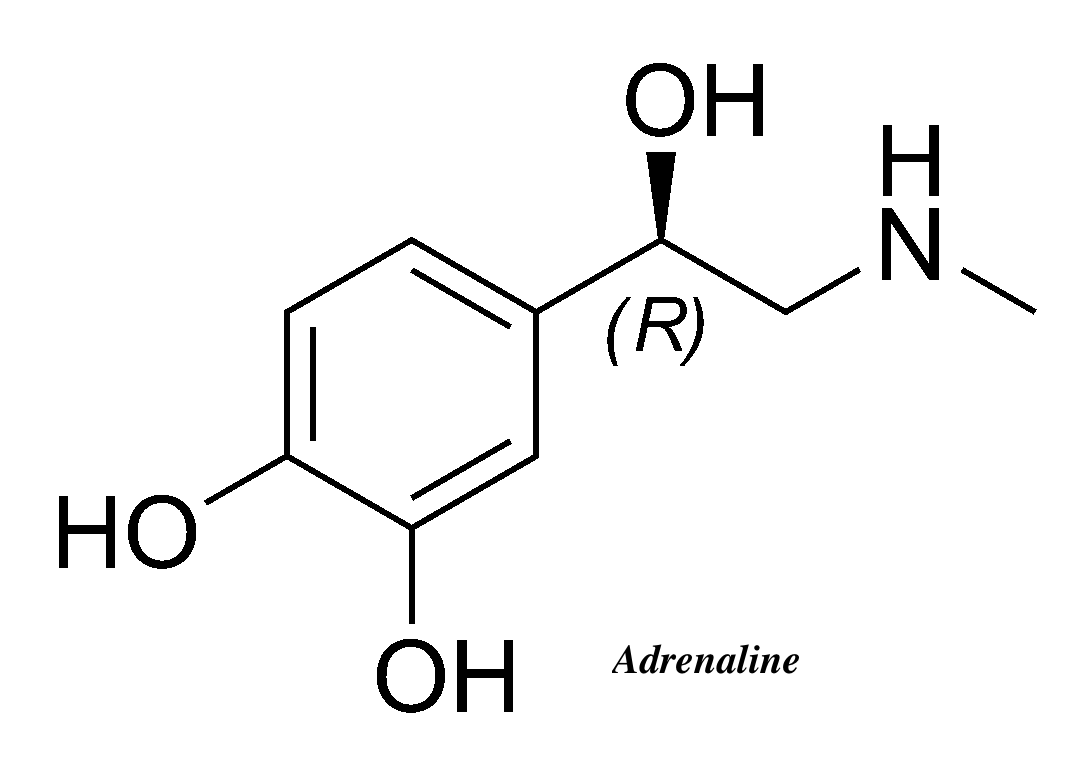
☆アドレナリンとは?
「アドレナリンとは、腎臓の上にある副腎 というところの中の髄質から分泌されるホルモンです。主な作用は、心拍数や血圧上昇などがあります。 自律神経の交感神経が興奮することによって分泌が高まります。その結果、主な作用として、心拍数や血圧上昇が上昇し、体のパフォーマンスが高まります。 また、覚醒作用があり、集中力や注意力も高まります。アドレナリンが分泌されることにより、目の前の恐怖や不安に対して、体と脳が戦闘モードに切り替わ り、立ち向かうことができるのです。」https://kentei.healthcare/column/2207/
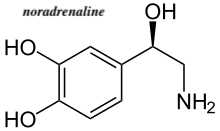
☆ノルアドレナリン
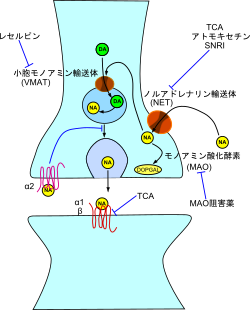
「ノルアドレナリンは、脳内の神経伝達物 質、自律神経の神経伝達物質、副腎髄質から分泌されるホルモンとしての3つの役割があります。 ノルアドレナリンの分泌を促すものは、痛み、かゆみ、寒暖差、人間関係などのストレスがあります。アドレナリンと同じく、目の前の恐怖や不安に対して、体 と脳が戦闘モードに切り替わり、立ち向かうことができるのです。そのため、集中力を高めたり、積極性な行動を起こすことにも役立ちます。 ノルアドレナリンが不足すると、やる気や集中力が低下してしまいます。また、逆にノルアドレナリンが過剰に分泌されると「パニック障害」を引き起こす原因 になるといわれています。」https://kentei.healthcare/column/2207/
「ノルアドレナリン系における変化 は憂うつに関係する。SNRIは、脳内のシナプス後細胞で、利用可能なセロトニンとノルアドレナリンの量を増加させることによって、うつを治療する。最近 はノルアドレナリン自己受容体がドーパミンも再取り込みするかもしれないという仮説では、これはSNRI(セロトニン・ノルアドレナリン再取り込み阻害 薬: Serotonin & Norepinephrine Reuptake Inhibitors; SNR)がドーパミン伝達をも増加させるかもしれないことを意味する。 一部の他の抗うつ薬[注釈 1]もまた、ノルアドレナリンに影響する。いくつかの場合、他の神経伝達物質に影響しない[注釈 2]。ノルアドレナリンはアミノ酸チロシンから一連の酵素反応を経て合成される。最初のレボドパ (L-DOPA) への酸化の後に神経伝達物質ドーパミンへの脱炭酸が続き、ドーパミン-β-モノオキシゲナーゼによりノルアドレナリンへ酸化される。さらにノルアドレナリ ンはアドレナリンへメチル化できる。」https://x.gd/w1oTn.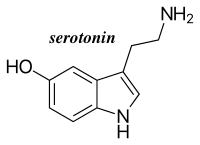
★アドレナリンとノルアドレナリンの違い
「ノルアドレナリンとアドレナリンの最も 大きな違いは、脳への精神的な作用の有無です。ノルアドレナリンは、脳内で神経伝達物質として分泌されるため、恐怖や怒り、不安などの精神的な作用にかか わっています。一方、アドレナリンは脳内ではほとんど分泌されず、また、副腎髄質で分泌されたアドレナリンは血液脳関門を通過することができないため、精 神的な作用には関与していません。 ノルアドレナリンは神経伝達物質、アドレナリンはホルモンとして紹介されていることがありますが、これは分泌量や作用として主に働く場所を指しているため です。」https://kentei.healthcare/column/2207/
☆ドーパミンとは
「ドーパミン(英: dopamine)は、中枢神経系に存在する神経伝達物質で、アドレナリン、ノルアドレナリンの前駆体でもある。運動調節、ホルモン調節、快の感情、意 欲、学習などに関わる。セロトニン、ノルアドレナリン、アドレナリン、ヒスタミン、ドーパミンを総称してモノアミン神経伝達物質と呼ぶ。またドーパミン は、ノルアドレナリン、アドレナリンと共にカテコール基をもつためカテコールアミンとも総称される。統合失調症の陽性症状(幻覚・妄想など)は基底核や中 脳辺縁系ニューロンのドーパミン過剰によって生じるという仮説がある。この仮説に基づき薬物療法で一定の成果を収めてきているが、一方で陰性症状には効果 が無く、根本的病因としては仮説の域を出ていない。覚醒剤はドーパミン作動性に作用するため、中毒症状は統合失調症に類似する。強迫性障害、トゥレット障 害、注意欠陥多動性障害 (ADHD) においてもドーパミン機能の異常が示唆されている。中脳皮質系ドーパミン神経は、とくに前頭葉に分布するものが報酬系などに関与し、意欲、動機、学習など に重要な役割を担っていると言われている。新しい知識が長期記憶として貯蔵される際、ドーパミンなどの脳内化学物質が必要になる[5]。陰性症状の強い統 合失調症患者や、一部のうつ病では前頭葉を中心としてドーパミンD1の機能が低下しているという仮説がある。」https://x.gd/LGcv1.
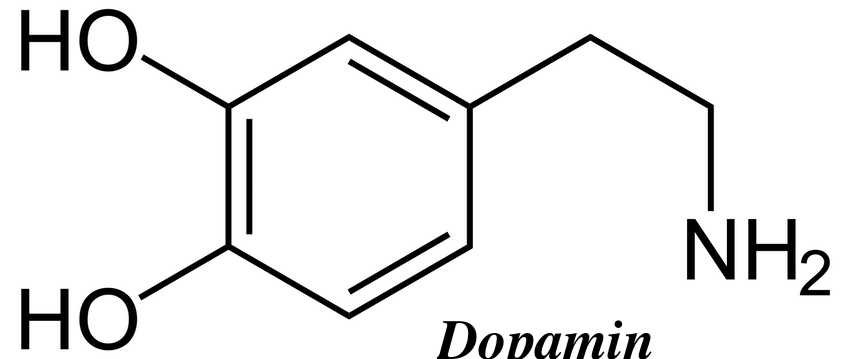
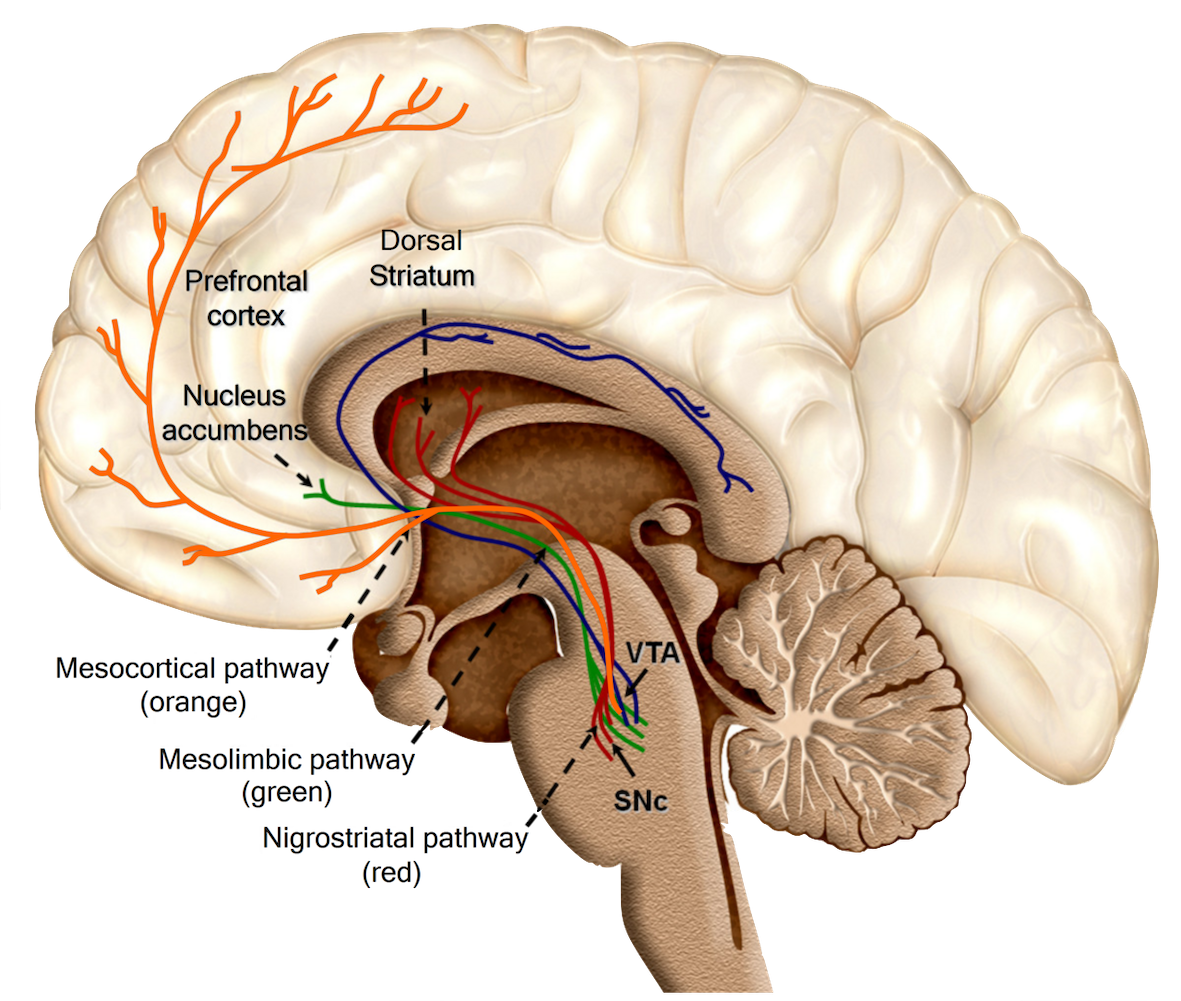
Diagram showing some of the key components of the mesocorticolimbic ("reward") circuit; Ventral tegmental area /中脳皮質辺縁系(報酬系)回路の主要な構成要素を示す図。腹側被蓋野
「報酬系(the Reward system) は、動物が刺激に近づいたり、体力を高める行動(セックス、エネルギー密度の高い食物など)をとったりする動機付けとなる。ほとんどの動物種の生存は、有 益な刺激との接触を最大化し、有害な刺激との接触を最小化することに依存している。報酬認知は、連合学習を引き起こし、接近行動や消費行動を誘発し、正の 価値で評価された情動を引き起こすことによって、生存と繁殖の可能性を高める役割を果たす。このように、報酬は動物の適応適性を高めるために進化したメカ ニズムである。薬物中毒では、ある種の物質が報酬回路を過剰に活性化し、回路内のシナプス可塑性の結果、強迫的な物質探索行動を引き起こす。一次報酬は、 自己と子孫の生存を促進する報酬刺激の一種で、恒常性維持報酬(例えば、口当たりのよい食物)と生殖報酬(例えば、性的接触や親からの投資)が含まれる。 内発的報酬とは、魅力的であり、本質的に快楽的であるために行動の動機づけとなる無条件の報酬であり、外発的報酬(例えば、金銭や好きなスポーツチームが 試合に勝つのを見ること)とは、魅力的であり、行動の動機づけとなるが、本質的に快楽的ではない条件付きの報酬である。外在的報酬は、内在的報酬との学習 された関連付け(すなわち、条件付け)の結果として、動機づけの価値を導き出す。外在的報酬もまた、内発的報酬と古典的に条件づけられた後に、快楽(例え ば、宝くじで大金が当たったときの陶酔感)を引き出すことがある。」Reward system)。
| Key
pathway of the
Reward system. The ventral tegmental area (VTA) is important in responding to stimuli and cues that indicate a reward is present. Rewarding stimuli (and all addictive drugs) act on the circuit by triggering the VTA to release dopamine signals to the nucleus accumbens, either directly or indirectly.[citation needed] The VTA has two important pathways: The mesolimbic pathway projecting to limbic (striatal) regions and underpinning the motivational behaviors and processes, and the mesocortical pathway projecting to the prefrontal cortex, underpinning cognitive functions, such as learning external cues, etc.[31] Dopaminergic neurons in this region converts the amino acid tyrosine into DOPA using the enzyme tyrosine hydroxylase, which is then converted to dopamine using the enzyme dopa-decarboxylase.[32] |
主要経路 腹側被蓋野(VTA)は、報酬の存在を示す刺激や合図に反応する上で重要である。報酬刺激(およびすべての中毒性薬物)は、VTAが側坐核にドーパミン・ シグナルを放出するよう、直接的または間接的に誘発することによって、この回路に作用する: 大脳辺縁系(線条体)領域に投射され、動機づけ行動やプロセスを支える中辺縁系経路と、前頭前皮質に投射され、外部からの手がかりを学習するなどの認知機 能を支える中皮質系経路である[31]。 この領域のドーパミン作動性ニューロンは、酵素チロシンヒドロキシラーゼを用いてアミノ酸チロシンをDOPAに変換し、次いで酵素ドーパデカルボキシラー ゼを用いてドーパミンに変換する[32]。 |
| Striatum (Nucleus Accumbens) The striatum is broadly involved in acquiring and eliciting learned behaviors in response to a rewarding cue. The VTA projects to the striatum, and activates the GABA-ergic Medium Spiny Neurons via D1 and D2 receptors within the ventral (Nucleus Accumbens) and dorsal striatum.[33] The Ventral Striatum (the Nucleus Accumbens) is broadly involved in acquiring behavior when fed into by the VTA, and eliciting behavior when fed into by the PFC. The NAc shell projects to the pallidum and the VTA, regulating limbic and autonomic functions. This modulates the reinforcing properties of stimuli, and short term aspects of reward. The NAc Core projects to the substantia nigra and is involved in the development of reward-seeking behaviors and its expression. It is involved in spatial learning, conditional response, and impulsive choice; the long term elements of reward.[31] The Dorsal Striatum is involved in learning, the Dorsal Medial Striatum in goal directed learning, and the Dorsal Lateral Striatum in stimulus-response learning foundational to Pavlovian response.[34] On repeated activation by a stimuli, the Nucleus Accumbens can activate the Dorsal Striatum via an intrastriatal loop. The transition of signals from the NAc to the DS allows reward associated cues to activate the DS without the reward itself being present. This can activate cravings and reward-seeking behaviors (and is responsible for triggering relapse during abstinence in addiction).[35] |
線条体(扁桃核) 線条体は、報酬的な手がかりに反応する学習行動の獲得と誘発に広く関与している。VTAは線条体に投射し、腹側(側坐核)および背側線条体内のD1および D2受容体を介してGABA作動性中棘神経を活性化する[33]。 腹側線条体(扁桃核)は、VTAから入力された場合は行動の獲得に、PFCから入力された場合は行動の誘発に広く関与している。NAc殻は淡蒼球とVTA に投射し、大脳辺縁系と自律神経機能を調節している。これは刺激の強化特性と報酬の短期的側面を調節する。NAcコアは黒質に投射し、報酬を求める行動の 発達とその発現に関与する。NAcコアは、空間学習、条件反応、および衝動的選択に関与しており、報酬の長期的要素である[31]。 背側線条体は学習に、背内側線条体は目標指向性学習に、背外側線条体はパブロフ反応の基礎となる刺激反応学習に関与している[34]。刺激による反復活性 化において、扁桃核は線条体内ループを介して背側線条体を活性化することができる。NAcから線条体へのシグナルの移行により、報酬そのものが存在しなく ても、報酬に関連する合図が線条体を活性化する。これにより、渇望や報酬を求める行動が活性化される(そして、依存症における断薬中の再発の引き金とな る)[35]。 |
| Prefrontal Cortex The VTA dopaminergic neurons project to the PFC, activating glutaminergic neurons that project to multiple other regions, including the Dorsal Striatum and NAc, ultimately allowing the PFC to mediate salience and conditional behaviors in response to stimuli.[35] Notably, abstinence from addicting drugs activates the PFC, glutamatergic projection to the NAc, which leads to strong cravings, and modulates reinstatement of addiction behaviors resulting from abstinence. The PFC also interacts with the VTA through the mesocortical pathway, and helps associate environmental cues with the reward.[35] |
前頭前皮質 VTAドーパミン作動性ニューロンはPFCに投射し、背側線条体やNAcを含む他の複数の領域に投射するグルタミン作動性ニューロンを活性化し、最終的に PFCが刺激に対する顕著性と条件行動を媒介することを可能にする[35]。 注目すべきは、中毒性薬物を断薬するとPFCが活性化され、NAcへのグルタミン酸作動性投射が強い渇望を引き起こし、断薬による中毒行動の復調が調節さ れることである。PFCはまた、中脳皮質経路を介してVTAと相互作用し、環境的手がかりと報酬の関連付けを助ける[35]。 |
| Hippocampus The Hippocampus has multiple functions, including in the creation and storage of memories . In the reward circuit, it serves to contextual memories and associated cues. It ultimately underpins the reinstatement of reward-seeking behaviors via cues, and contextual triggers.[36] |
海馬 海馬は、記憶の創造と保存を含む複数の機能を持っている。報酬回路では、海馬は文脈記憶と関連する手がかりの役割を果たす。海馬は最終的に、手がかりや文 脈上の誘因を介して、報酬を求める行動の復調を支える[36]。 |
| Amygdala The AMY receives input from the VTA, and outputs to the NAc. The amygdala is important in creating powerful emotional flashbulb memories, and likely underpins the creation of strong cue-associated memories.[37] It also is important in mediating the anxiety effects of withdrawal, and increased drug intake in addiction.[38] |
扁桃体 扁桃体はVTAから入力を受け、NAcに出力する。扁桃体は、強力な情動的フラッシュバルブ記憶を創り出すのに重要であり、おそらく強力な手がかり関連記 憶の創出を支えている。 |
| Pleasure centers Pleasure is a component of reward, but not all rewards are pleasurable (e.g., money does not elicit pleasure unless this response is conditioned).[1] Stimuli that are naturally pleasurable, and therefore attractive, are known as intrinsic rewards, whereas stimuli that are attractive and motivate approach behavior, but are not inherently pleasurable, are termed extrinsic rewards.[1] Extrinsic rewards (e.g., money) are rewarding as a result of a learned association with an intrinsic reward.[1] In other words, extrinsic rewards function as motivational magnets that elicit "wanting", but not "liking" reactions once they have been acquired.[1] The reward system contains pleasure centers or hedonic hotspots – i.e., brain structures that mediate pleasure or "liking" reactions from intrinsic rewards. As of October 2017, hedonic hotspots have been identified in subcompartments within the nucleus accumbens shell, ventral pallidum, parabrachial nucleus, orbitofrontal cortex (OFC), and insular cortex.[2][17][39] The hotspot within the nucleus accumbens shell is located in the rostrodorsal quadrant of the medial shell, while the hedonic coldspot is located in a more posterior region. The posterior ventral pallidum also contains a hedonic hotspot, while the anterior ventral pallidum contains a hedonic coldspot. In rats, microinjections of opioids, endocannabinoids, and orexin are capable of enhancing liking reactions in these hotspots.[2] The hedonic hotspots located in the anterior OFC and posterior insula have been demonstrated to respond to orexin and opioids in rats, as has the overlapping hedonic coldspot in the anterior insula and posterior OFC.[39] On the other hand, the parabrachial nucleus hotspot has only been demonstrated to respond to benzodiazepine receptor agonists.[2] Hedonic hotspots are functionally linked, in that activation of one hotspot results in the recruitment of the others, as indexed by the induced expression of c-Fos, an immediate early gene. Furthermore, inhibition of one hotspot results in the blunting of the effects of activating another hotspot.[2][39] Therefore, the simultaneous activation of every hedonic hotspot within the reward system is believed to be necessary for generating the sensation of an intense euphoria.[40] |
快楽中枢 快楽は報酬の構成要素であるが、すべての報酬が快楽的であるわけではない(例えば、この反応が条件付けされない限り、お金は快楽を引き出さない)[1]。 自然に快楽的であり、したがって魅力的な刺激は内在的報酬と呼ばれ、魅力的で接近行動を動機付けるが、本質的に快楽的ではない刺激は外在的報酬と呼ばれる [1]、 言い換えれば、外発的報酬は、いったん獲得されると「欲しい」という反応は引き出すが「好き」という反応は引き出さない動機づけの磁石として機能する [1]。 報酬系には快感中枢または快感ホットスポット、すなわち内発的報酬による快感や「好き」反応を媒介する脳構造が存在する。2017年10月現在、快楽性 ホットスポットは、側坐核殻、腹側淡蒼球、傍上腕核、眼窩前頭皮質(OFC)、および島皮質内のサブコンパートメントで同定されている[2][17] [39]。側坐核殻内のホットスポットは内側殻の吻背側四分円に位置し、快楽性コールドスポットはより後方の領域に位置する。腹側淡蒼球後部にも快楽ホッ トスポットがあり、腹側淡蒼球前部には快楽コールドスポットがある。ラットにおいて、オピオイド、エンドカンナビノイド、オレキシンの微量注射は、これら のホットスポットにおける嗜好反応を増強することができる。 [39] 一方、傍上腕核ホットスポットはベンゾジアゼピン受容体作動薬にのみ反応することが証明されている[2]。 ヘドニックホットスポットは機能的に関連しており、1つのホットスポットを活性化すると、即時型遺伝子であるc-Fosの発現誘導によって指標されるよう に、他のホットスポットも動員される。さらに、1つのホットスポットを抑制すると、他のホットスポットを活性化する効果が鈍くなる[2][39]。した がって、報酬系内のすべての快楽性ホットスポットが同時に活性化されることが、強烈な多幸感の感覚を生み出すために必要であると考えられている[40]。 |
| https://en.wikipedia.org/wiki/Reward_system |
リンク
文献
その他の情報
Copyleft, CC, Mitzub'ixi Quq Chi'j, 1997-2099
**
Copyleft, CC, Mitzub'ixi Quq Chi'j, 1996-2099
☆
 ☆
☆